问题
选择题
今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH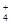 、Ba2+、Cl-、CO
、Ba2+、Cl-、CO 、SO
、SO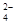 。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,以下推测正确的是
。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,以下推测正确的是
A.一定不存在Ba2+,NH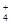 可能存在
可能存在
B.CO 一定不存在
一定不存在
C.Na+一定存在
D.一定不存在Cl-
答案
答案:C
根据实验①可知,溶液中一定含有NH4+。氨气是1.36g,物质的量是0.08mol,则NH4+也是0.08mol;根据实验②可知,硫酸钡的质量是4.66g,碳酸钡的质量是12.54g-4.66g=7.88g,物质的量分别是0.02mol和0.04mol,则溶液中SO42-和CO32-的物质的量分别是0.02mol和0.04mol。所以溶液中一定没有Ba2+。根据溶液的电中性可知,溶液中一定还含有钠离子,但氯离子是不能确定的,选项C正确,答案选C。
