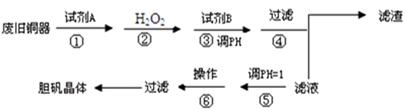
(16分)胆矾是一种重要工业用盐,如电镀工业用作全光亮酸性镀铜主盐和铜离子添加剂。印染工业用作媒染剂和精染布的助氧剂。农业上作为杀菌剂。某研究小组拟用废旧铜器(主要杂质为含铁的化合物)来制备胆矾。设计流程如下:
pH值控制可参考下列数据
| 物质 | 开始沉淀时的pH值 | 完全沉淀时的pH值 |
| 氢氧化铁 | 2.7 | 3.7 |
| 氢氧化亚铁 | 7.6 | 9.6 |
| 氢氧化铜 | 5.2 | 6.4 |
(1)试剂A可选用_____(填字母)。
a.稀H2SO4 b.浓H2SO4 c.浓FeCl3溶液 d.浓HNO3
(2)第②步加入H2O2溶液发生的反应的离子方程式为:_____________________________。
(3)第③步中所加试剂B为________(填化学式)。调节溶液的pH合适的范围是__________。
(4)操作⑤通常加H2SO4调节pH=1是为了:______________________________________。
(5)本流程中多次用到过滤操作,该操作主要用到的玻璃仪器为: _______________,操作⑥的主要步骤为: 、 。
(6)某同学认为上述流程中所加的试剂A并不理想,需作改进,其理由是______________
__________________________________________________________。请你帮助提出一条改进方案____________ 。
(1)b;
(2)2Fe2++H2O2+2H+=2Fe3++2H2O (2分)
(3)CuO或Cu(OH)2或Cu2(OH)2CO3等合理答案。(1分) PH:3.7—5.2(2分)
(4)抑制Cu2+水解
(5)漏斗、烧杯、玻璃棒等;(2分) 蒸发浓缩,冷却洁净(各1分)
(6)产生污染环境的二氧化硫,硫酸利用率低;(2分)加热,并在稀硫酸中通入氧气。(2分)
本题来源于真实的化工工艺,废旧电器的综合得用。以废旧铜器为原料,制备重要工业用盐胆矾为主线,综合考查元素化合物的性质、离子反应、沉淀的生成和溶解、过滤、溶液酸碱性(pH)的应用、盐类水解、重结晶等基础知识;考查学生调控化学实验条件的能力、观察和分析图表的能力。
从流程来看①是加入浓硫酸,将铜溶解为铜离子,同时铁的化合物以二价或三价进入溶液。第②步加入H2O2溶液,将二价铁氧化为三价铁,第③步再加入CuO调pH到3.7~5.2之间,过滤除去氢氧化铁(滤渣),铜离子留在溶液。为了防止铜离子在加热浓缩时水解,加入硫酸控制酸度,抑制水解。当溶液浓缩到一定程度,冷却即可结晶出胆矾,过滤即得产品。第(6)小题要求较高,主要是考查考生对简单实验设计的评价或改进的能力。从绿色化学理念来看,加入浓硫酸与铜反应会产生污染环境的二氧化硫,硫酸利用率也较低;可考虑在加热的条件下,加入稀硫酸,同时通入氧气。上述问题得以解决。本小问回答有一定的开放性,给不同水平的考生以施展能力的空间。
