(3分)某化学调查小组的同学到钢铁厂做社会调查。他们抽取组成完全相同的质量为2.84g、4.26g、6.23g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制成如下图像:
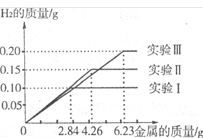
(1)实验I中铁参加反应的质量为 。
(2)稀硫酸完全参加反应的实验中,反应后溶液中溶质的质量分数是多少。
(1)2.8克(1分)(2)14.4%(2分)
题目分析:(1)由题意可知,实验I中反应完全后生成氢气的质量是0.1g。
解:设实验I中铁参加反应的质量为X;反应生成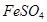 的质量为Y。
的质量为Y。
Fe+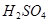 =
=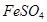 +
+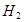 ↑
↑
56 2
X 0.1g
56:2=X:0.1g
X=2.8g
(2)由题意可知,100g稀硫酸与6.23g样品完全恰好反应。
解:设稀硫酸完全参加反应的实验中,生成的硫酸亚铁的质量为Y。
Fe+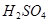 =
=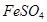 +
+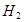 ↑
↑
152 2
Y 0.2g
152:2=Y:0.2g
Y=15.2g
稀硫酸完全参加反应的实验中,反应后溶液中溶质的质量分数是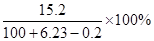 =14.4%
=14.4%
答:(1)实验I中铁参加反应的质量为2.8g;
稀硫酸完全参加反应的实验中,反应后溶液中溶质的质量分数是14.4%。
点评:根据化学方程式计算,要注意解题的步骤,设、写、找、列、解、答。
溶液中溶质的质量分数=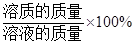 。
。