问题
计算题
如图所示,将0.1mol氧化铜与一定量的碳混合加热,充分反应(试管中的空气已被除去)。
(1)计算该实验最多可以生成多少克二氧化碳?(请根据化学方程式列式计算)

(2)实验前后分别称量了装置A和装置B的质量如表中所示。若数据Ⅰ准确,请回答:
a反应后A中固体的成分是_ 。
b数据Ⅱ存在的问题是_ ,可能的原因是 。
| 反应前质量(g) | 反应后质量(g) | ||
| Ⅰ | 装置A | 125.3 | 124.2 |
| Ⅱ | 装置B | 152 | 152.3 |
答案
(1)2.2g;(2)a氧化铜和铜 b数据Ⅱ中反应后的质量偏小 澄清石灰水量不足,没有将生成的二氧化碳全部吸收
题目分析: 解;设生成二氧化碳的物质的量为x
C+2CuO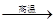 2Cu+CO2
2Cu+CO2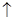
2 1
0.1 x
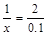
X="0.05" )
0.05mol ×44g/mol="2.2g"
②如完全反应质量应该减少2.2g,而实际减少了125.3g-124.2g=1.1g,剩余氧化铜,反应后A中固体的成分是氧化铜和铜 因为生成了二氧化碳1.1g, Ⅱ中只增加了0.3g,故数据Ⅱ中反应后的质量偏小,可能的原因是澄清石灰水量不足,没有将生成的二氧化碳全部吸收(合理给分)可能的原因是
