某温度下向20mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 mol·L-1 NaOH溶液,混合液的pH随NaOH溶液的体积(V)的变化关系如图(忽略温度变化)。下列说法中正确的是( )
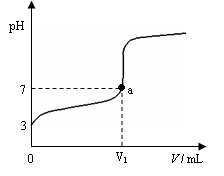
A.该温度下醋酸的电离平衡常数约为1×10-5mol·L-1
B.图中V1 > 20mL,且a点对应的溶液中:
c (Na+)+ c (H+) = c (OH-)+ c (CH3COO-)
C.图中V1 < 20mL,且a点对应的溶液中:
c (CH3COOH) + c (CH3COO-)<c (Na+)
D.当加入Na OH溶液的体积为20mL时,溶液中:c (CH3COOH) + c (H+) > c (OH-)
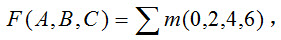 则可以写为()。
则可以写为()。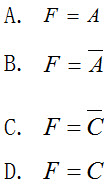
 则可以写为()。
则可以写为()。