问题
问答题
环宇公司2005年有关销售及现金收支情况见下表:
销售及现金收支情况表 单位:元
| 项 目 | 第一季度 | 第二季度 | 第三季度 | 第四季度 | 合计 |
| 产品销售量 | 3 000 | 4 000 | 5 500 | 6 000 | 18 500 |
| 销售单价 | 100 | 100 | 100 | 100 | 100 |
| 期初现金余额 | 21 000 | ||||
| 经营现金流出 | 261 800 | 298 100 | 354 000 | 593 300 | 1 507 200 |
(1)销售税金及附加估计税率为5.5%;
(2)该公司期初应收账款为80 000元,其中第四季度销售形成的应收账款为50 000元;
(3)该公司历史资料显示:当季销售当季收回现金60%,下季收回现金30%,第三季度收回现金10%;
(4)该公司最佳现金余额为6 000元。
(5)银行借款按期初借款、期末还款处理,借款利率为10%(利随本清法);
(6)资金筹措和运用按500元的倍数进行;
(7)该公司期初有证券投资5 000元,资金余缺的调整可通过买卖证券来进行,以减少负债为基本目的;
(8)经营现金流出量中不包括销售环节税金现金流出量。
要求:根据上述资料编制销售预算表及现金预算表。
答案
参考答案:[答案及解析]
根据上述资料编制销售预算表。
销售预算 单位:元
| 项 目
填空题
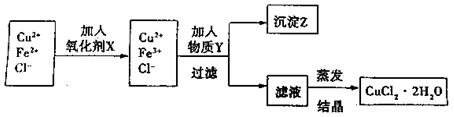
(15分)制取纯净的氯化铜晶体(CuCl2·2H2O)的生产过程如下: I.将粗氧化铜(含少量Fe)溶解在足量的稀盐酸中,然后加热、过滤得到CuCl2(含少量FeCl2)溶液,经测定,溶液pH为2。 II.对I中所得到的溶液按下列步骤进行提纯。
已知:
(1)下列物质中,最适合作为氧化剂X的是 A.KMnO4 B.K2Cr2O4 C.H2O2 D.NaClO (2)①加紧入的物质Y是 ②写出沉淀Z在水中的沉淀溶解平衡方程式: 。 (3)分离出沉淀Z,并将滤液蒸发,欲获得氯化铜晶体(CuCl2·2H2O),应采取的措施是 。 (4)①某同学利用反应:Cu+2H+===Cu2 ②请你在下面方框中画出该同学设计的装置图,并指明电极材料和电解质溶液。
(5)已知一些难溶物的浓度积常数如下表:
①NaOH ②FeS ③Na2S |

 始沉淀时的pH
始沉淀时的pH 。(填序号)
。(填序号) ++H2↑设计实验来制取CuCl2溶液,该同学设计的装置应该为 。(填“原电池”或“电解池”)
++H2↑设计实验来制取CuCl2溶液,该同学设计的装置应该为 。(填“原电池”或“电解池”)