一种白色晶体A极易溶于水,将A配成溶液进行如下框图所示的实验,实验现象及转化关系如下列框图所示.
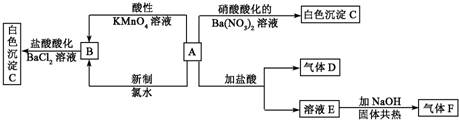
其中A为正盐,气体D能使品红溶液褪色,气体F能使湿润的红色石蕊试纸变蓝.试回答下列问题:
(1)写出下列物质化学式:A:______;C:______;
(2)写出下列反应的离子方程式:
①由B生成C:______②气体D通入新制氯水:______③溶液E与固体NaOH共热生成气体F:______.
根据已知条件:能使品红溶液褪色的是二氧化硫,所以D是二氧化硫,能使湿润的红色石蕊试纸变蓝的是氨气,即F是氨气,A是一种白色晶体,和其他物质反应既能生成氨气又能生成二氧化硫,所以A是(NH4)2SO3,容易被氧化剂氧化为硫酸铵,所以B是硫酸铵,得出E是氯化铵.
白色沉淀C是硫酸钡,
(1)能和其他物质反应既能生成氨气又能生成二氧化硫的白色晶体是(NH4)2SO3,硫酸铵和氯化钡发生复分解反应生成硫酸钡沉淀,所以C是BaSO4,故答案为:(NH4)2SO3;BaSO4;
(2)①钡离子和硫酸根能反应,离子方程式为:Ba2++SO42-=BaSO4↓,故答案为:Ba2++SO42-=BaSO4↓;
②氯气能将二氧化硫氧化,离子方程式为:SO2+Cl2+2H2O=SO42-+4H++2Cl-,故答案为:SO2+Cl2+2H2O=SO42-+4H++2Cl-;
③铵盐和强碱共热会生成氨气,是一种碱性气体,原理为NH4++OH-
NH3↑+H2O,故答案为:NH4++OH- △ .
NH3↑+H2O. △ .
