根据下列材料,按要求完成任务。
材料一《义务教育化学课程标准(2011年版)》的内容标准:能正确书写简单的化学反应方程式,并进行简单的计算。
材料二教科书的知识结构体系
绪言化学使世界变得更加绚丽多彩
第一单元走进化学世界
第二单元我们周围的空气
第三单元物质构成的奥秘
第四单元自然界的水
第五单元化学方程式
课题1质量守恒定律
课题2如何正确书写化学方程式
课题3利用化学方程式的简单计算
第六单元碳和碳的氧化物
第七单元燃料及其利用
第八单元金属和金属材料
第九单元溶液
第十单元酸和碱
第十一单元盐化肥
第十二单元化学与生活
材料三人教版初中《化学》“如何正确书写化学方程式”部分教材内容。
化学方程式反映化学反应的客观事实。因此,书写化学方程式要遵守两个原则:一是必须以客观事实为基础,绝不能凭空臆想、臆造事实上不存在的物质和化学反应;二是要遵守质量守恒定律,等号两边各原子的种类与数目必须相等。
木炭在氧气中燃烧生成二氧化碳的化学方程式:
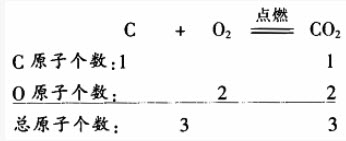
该化学方程式等号两边的原子种类和数目都相等,这个化学方程式我们称配平了。但并不是所有的化学方程式都这么简单。例如,氢气与氧气反应生成水:
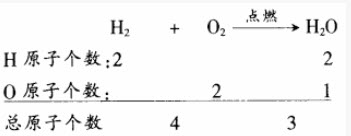
在这个式子中.右边的氧原子数少于左边的,这时为使式子两边每一种元素原子的总数相等,就需要配平.即在式子两边的化学式前面配上适当的化学计量数。

在H前配上2,在HO前配上2,式子两边的H原子、O原子数目就都相等了,亦即化学方程式配平了。
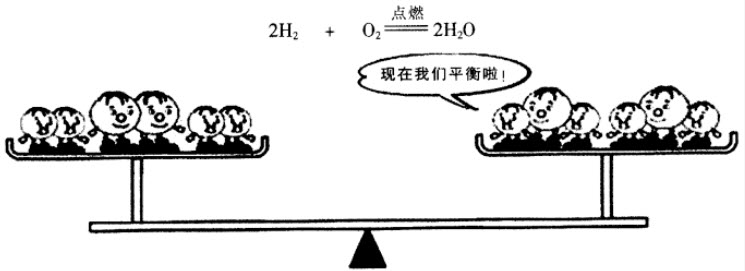
下面以磷在空气中燃烧生成五氧化二磷的反应为例,说明书写化学方程式的具体步骤。
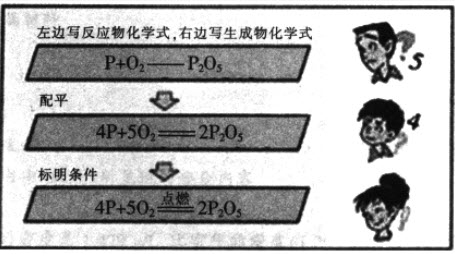
1.根据实验事实,在式子的左、右两边写出反应物和生成物的化学式,并在式子左、右两边之间画一条短线(或标出一个指向生产物的箭头)。

2.配平化学方程式,并检查。

3.标明化学反应发生的条件,把短线改成等号。

化学反应只有在一定条件下才能发生,因此,需要在化学方程式中注明反应发生的条件。如把点燃、加热(常用“△”号表示)、催化剂等,写在等号的上方。
如果生成物中有气体,在气体物质的化学式右边要注“↑”号;溶液中的反应如果生成物中有固体,在固体物质的化学式右边要注“↓”号。例如:
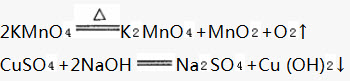
但是.如果反应物和生成物中都有气体,气体生成物就不需注“↑”号。同样,溶液中的反应物如果反应物和生成物中都有固体,固体生成物也不需注“↓”号。例如:
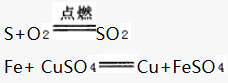
任务:
(1)对本课内容进行学情分析。
(2)试确定本课的三维教学目标。
(3)试确定本课的教学重点与难点。
(4)请对本课内容进行教学过程设计。
参考答案
【答案
参考答案:
(1)从教材体系上看,《如何正确书写化学方程式》这个课题是元素符号、化学式等知识的延伸和扩展,并与元素符号、化学式构成了九年级化学三个重要的化学用语。它在本单元中是联系质量守恒定律和进行化学计算的“中介”,是进行化学计算的基础,也是整个初中化学教学的重点之一,是学生学好化学的前提和保证,更是解决化学问题的最重要的工具。在前面的学习中,学生已经学习了元素、分子、原子、化学式、化合价等相关基础知识,学会书写元素符号、化学式等;在课题1中,学生刚刚学习了质量守恒定律,认识了化学方程式的意义及所能提供的信息,这些为本节课学习正确书写化学方程式奠定了基础。化学方程式的书写是化学学习中的重要技能,难度并不大,但因涉及元素符号、化学式的书写等内容.如果学生在前面的学习中存在困难,本节内容很可能成为其学习的难点。
(2)教学目标
知识与技能目标:了解书写化学方程式应遵循的原则;会用化学方程式正确表达一般的化学反应。
过程与方法目标:认识科学探究的意义和基本过程,能发现问题,进行初步的探究活动;通过学生合作探究和自主探究,培养学生发现规律、认识规律和运用规律,培养学生科学的思维方法。
情感态度与价值观目标:结合化学方程式书写原则的教学,让学生形成实事求是的科学态度;克服书写上的随意性和盲目性,养成良好的习惯,不断培养全面思考问题的能力。
(3)教学重点与难点
教学重点:化学方程式的书写原则与配平方法。
教学难点:化学方程式的配平。
(4)教学过程
【创设情景,引出课题】
[投影]多媒体展示flash动画“剑桥之旅”。
[提问]他是如何开车顺利到达目的地——剑桥大学的呢?
[生答]根据路标、站牌等。(得出路标、站牌都是国际通用的交通语言。)
『提问]在我们变化无穷的化学世界里,对于同一个化学反应,不同的国家就有不同的表示方法。是否也有一种国际通用的表达方式呢?
[展示]不同的表示方法。请学生对上述五种表达方式进行对比分析,找出化学方程式表达的优越性(简单方便,且国际通用),体会化学方程式书写的重要性,从而引出课题。
【师生互动,探究化学方程式的书写原则和书写步骤】
[展示]一些化学方程式。请学生回顾化学方程式所提供的信息。
[得出结论]化学方程式表示的两方面的信息:
①表示反应物、生成物、反应的条件及生成物的状态(质的信息)
②表示反应物和生成物之间量的关系(量的信息)
过渡:复习了化学方程式质和量两方面的信息,让学生进行逆向思维。
[分组活动]将学生分为6组,写出6个化学方程式。
①硫在氧气中燃烧;
②红磷在空气中燃烧:
③铁丝在氧气中燃烧:
④氯酸钾和二氧化锰混合加热制氧气;
⑤加热高锰酸钾制氧气;
⑥二氧化碳和澄清石灰水(有效成分为氢氧化钙)反应,生成碳酸钙沉淀和水。
教师对这一过程进行观察和指导。
[展示成果并自我检查]学生检查6组结果是否能准确地传递出反应物、生成物及反应的条件等信息。若有错误,由各组同学进行纠错、订正。
[提问]是否能将第一组的反应条件“点燃”改为“加热”,或将第三组的生成物“Fe3O4”改为“Fe2O3”呢?
[讨论]得出化学方程式的第一个书写原则:要遵守客观事实。
[提问]为什么要在化学式的前面配上适当的数字即化学计量数呢?
[回答]为了保证反应前后各种原子的种类和数目相等。
得出化学方程式的第二个书写原则:要遵守质量守恒定律。
[引申]针对第二组化学方程式P2+O2→PO5,进行讨论,找出使两边磷原子和氧原子个数都相等的方法。然后,由小组代表进行讲解。
[投影]教师评价后,通过多媒体课件演示最小公倍数法的配平方法,向学生说明其要点,并提供找元素的秘诀:两端各出现一次且原子数目较大的元素。
[引申]对于第五组这个反应,有更好的配平方法吗?观察式子左右两边钾原子、锰原子、氧原子个数分别是多少,它们之间有什么规律?
[讲解]配平时应该注意三点:不得更改化学式;化学计量数不能为分数;化学计量数互为最简整数比。
[自主学习]如何标注生成物的状态。阅读课本并完成上述方程式生成物的状态。
[小结]箭头都标在了生成物的一方。反应物中没有气体,而生成物中有气体,应在该气体化学式的右侧标有向上的箭头。溶液中有固体沉淀生成,应在该沉淀化学式的右侧标有向下的箭头。
[展示]播放向澄清石灰水中吹气的录像,让学生由实验现象加深理解“↓”符号的含义。
[概括总结,促进知识迁移]
①写出反应物和生成物的化学式(遵守客观事实);
②配平,将短线改为等号(遵守质量守恒定律);
③注明反应的条件、生成物的状态(遵守客观事实)。
[知识应用,获得信息反馈]
①配平一些化学方程式;②写出一些反应的化学方程式。