问题
选择题
在10 L密闭容器中,1 mol A和3 mol B在一定条件下反应:A(气)+xB(气)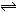 2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是
2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是
A.平衡时,物质的量比A∶B∶C=2∶11∶4
B.x值等于4
C.B的平均反应速率为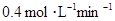
D.A的转化率20%
答案
AC
考查可逆反应的有关计算。
A(气)+xB(气)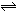 2C(气)
2C(气)
起始量(mol) 1 3 0
转化量(mol) 0.2 0.2x 0.4
平衡量(mol) 0.8 3-0.2x 0.4
所以有0.8+3-0.2x+0.4=3.4
解得x=4
所以平衡时,物质的量比A∶B∶C=4∶11∶2,A不正确,B正确。B的平均反应速率为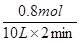 =
=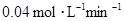 ,C不正确。A的转化率是0.2÷1×100%=20%,D正确,答案选AC。
,C不正确。A的转化率是0.2÷1×100%=20%,D正确,答案选AC。
