将4mol SO2(g)与2molO2(g)放入4L的密闭容器中,在一定条件下反应达到平衡:
2SO2(g)+ O2(g)  2SO3(g) 测得平衡时混合物总的物质的量为5mol,求:
2SO3(g) 测得平衡时混合物总的物质的量为5mol,求:
(1)平衡时各物质的浓度;
(2)平衡时SO2的转化率。
(10分)
解:设平衡时SO2转化的物质的量为2a
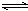 2SO2(g) + O2(g) 2SO3(g)
2SO2(g) + O2(g) 2SO3(g)
起始 4 mol 2 mol 0
转化 2a a 2a
平衡 4-2a 2-a 2a
4-2a+2-a+2a=5
a=1 (6分)
∴平衡时各物质的物质的量分别为
n(SO2)="2" mol n(O2)="1" mol n(SO3)="2" mol
∴平衡时各物质的物质的量浓度分别为
c(SO2)="0.5" mol/L c(O2)=0.25mol/L c(SO3)="0.5" mol/L (2分)
平衡时SO2的转化率="2" mol /4 mol×100%=50% (2分)
题目分析:解:设平衡时SO2转化的物质的量为2a
2SO2(g) + O2(g)  2SO3(g)
2SO3(g)
起始 4 mol 2 mol 0
转化 2a a 2a
平衡 4-2a 2-a 2a
4-2a+2-a+2a=5
a=1
∴平衡时各物质的物质的量分别为
n(SO2)="2" mol n(O2)="1" mol n(SO3)="2" mol
∴平衡时各物质的物质的量浓度分别为
c(SO2)="0.5" mol/L c(O2)=0.25mol/L c(SO3)="0.5" mol/L
平衡时SO2的转化率="2" mol /4 mol×100%=50%
点评:本题考查了三行式的应用;对于化学平衡的计算常用此法,学生要多加练习,此类问题便不难解决。