如下图所示,在容器A中装有20℃的水50 mL,容器B中装有1 mol/L的盐酸50 mL,试管C、D相连通,且其中装有红棕色NO2和无色N2O4的混合气体,并处于下列平衡:2NO2(g)  N2O4(g) ΔH=-57 kJ/mol,
N2O4(g) ΔH=-57 kJ/mol,
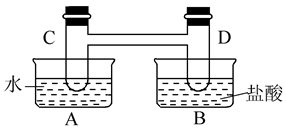
当向A中加入50 gNH4NO3晶体使之溶解;向B中加入2 g苛性钠时:
C中的气体颜色__________,D中的气体颜色__________(填“变浅”或“变深”)。
请简述原因 。
(2)若25℃时,起始时仅有NO2气体,反应2NO2 N2O4达到平衡时,c(NO2)=0.0125 mol/L,c(N2O4)=0.0321 mol/L,则NO2的起始浓度为__________,NO2的转化率为__________。
N2O4达到平衡时,c(NO2)=0.0125 mol/L,c(N2O4)=0.0321 mol/L,则NO2的起始浓度为__________,NO2的转化率为__________。
(8分)(1)变浅 变深 (每空1分)
在A中加入NH4NO3晶体时,温度降低,平衡向正反应方向移动,C中气体颜色变浅;在B中加入苛性钠时,温度升高,平衡向逆反应方向移动,D中气体颜色变深。(2分)
(2)0.076 7 mol/L 83.7%(每空2分)
题目分析:(1)该反应是放热反应,在A中加入NH4NO3晶体时,温度降低,平衡向正反应方向移动,C中气体颜色变浅;在B中加入苛性钠时,温度升高,平衡向逆反应方向移动,D中气体颜色变深。
(2)平衡时c(N2O4)=0.0321 mol/L,则根据方程式可知,消耗NO2的浓度是0.0321 mol/L×2=0.0642mol/L,所以NO2的起始浓度为0.0642mol/L+0.0125 mol/L=0.076 7 mol/L。NO2的转化率为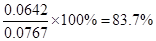 。
。
点评:该题是基础性试题的考查,难度不大。侧重对学生基础知识的巩固和训练,意在培养学生的逻辑推理能力,有利于提高学生的应试能力,增强学生的学习自信心。
