问题
选择题
已知:H2(g)+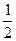 O2(g)=H2O(1) △H=-285.8kJ·mol-1
O2(g)=H2O(1) △H=-285.8kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(1)△H="-890.3" kJ·mol-1
现有H2和CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2(g)和H2O(1),共放出热精3242.5 kJ,则原混合气体中H2和CH4的物质的量之,比是 ( )
A.1:1
B.1:3
C.1:4
D.2:3
答案
答案:D
