问题
填空题
(5分)煤炭可以转化为清洁能源和化工原料。
(1)用煤可以制得水煤气。工业上可用煤和水通过水煤气法制氢气,已知下列热化学方程式:
C(s)+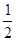 O2(g)=CO(g)
O2(g)=CO(g)  H1=-110.5 kJ/mol
H1=-110.5 kJ/mol
2H2(g)+O2(g)=2H2O(g)  H2=-483.6 kJ/mol
H2=-483.6 kJ/mol
试求水煤气法制氢气的反应的反应热 H3。
H3。
C(s)+H2O(g)=CO(g)+H2(g) H3= kJ/mol
H3= kJ/mol
(2)已知一氧化碳与水蒸气反应过程的能量变化如下图所示:则此反应为 (填“吸热”或“放热”)反应,反应的热化学方程式为 。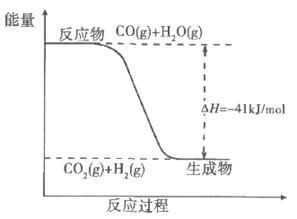
答案
(共5分) (1)+131.3(2分) (2)放热;
CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41 kJ/mol(2分,写高温条件不扣分)
(1)考查盖斯定律的应用。根据已知反应可知,①-②÷2即得到C(s)+H2O(g)=CO(g)+H2(g),所以反应热是-110.5 kJ/mol+483.6 kJ/mo÷2=+131.3 kJ/mol。
(2)根据图像可知,反应物的总能量高于生成物的总能量,所以是放热反应,放出的热量41 kJ,所以方程式为 CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41 kJ/mol。
