问题
计算题
硫铁矿高温下空气氧化产生二氧化硫:4FeS2+11O2→8SO2+2Fe2O3;设空气中N2、O2的含量分别为
0.800和0.200(体积分数,以下气体含量均用体积分数表示),试完成下列各题:
(1)1.00molFeS2完全氧化,需要空气的体积(标准状况)为______________L
(2)55L空气和足量FeS2完全反应后,气体体积(同温同压)变为______________L
(3)用空气氧化FeS2产生的气体混合物中,O2的含量为0.0800,SO2的含量为_______________
(4)设FeS2氧化产生的气体混合物为100L,其中O2为aL,SO2为bL。
① 写出a和b的关系式_______________
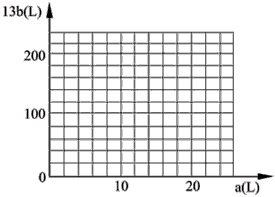
② 在图中画出a和b的关系曲线(FeS2氧化时,空气过量20%)
说明:为方便作图,纵坐标用13b表示
答案
(1)308
(2)52
(3)设SO2为X(体积分数),则有
4×(11×X/8+0.0800)=1-0.0800-X
X=0.0923
(4)13b=200-10a;画图“略”
