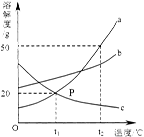
右图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
(1)P点的含义是 。
(2)t2℃时30g a物质加入到50g水中不断搅拌,能形成80g溶液吗? (填写“能”或“不能”)。
(3)t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是 (填写物质序号)。
(4)将t2℃时a、b、c三种物质等质量的饱和溶液降温到t1℃时,析出晶体最多的是 (填写物质序号)。
(5)将t2℃时a、b、c三种物质等质量的饱和溶液降温到t1℃时,所得溶液中溶质的质量分数由大到小的顺序是 (填写物质序号)。
(1)t1℃时a、c两种物质的溶解度相等
(2)不能
(3)c < b < a
(4)a
(5)b >a> c
题目分析:(1)P点是溶解度曲线图上的一点,表示在对应的温度时该物质的溶解度。该图中P点对应的温度为t1℃,对应的溶解度的值为20g;且为a、c两种物质的溶解度曲线的交点。所以其含义为t1℃时a、c两种物质的溶解度相等。均为20g。
(2)从图中可知:t2℃时a的溶解度为50g。即t2℃时在100g水中最多溶解a物质的质量为50g。当水为50g时,则最多溶解a的质量为25g。因此溶液质量为:25g(溶质质量)+50g(溶剂质量)=75g 所以不能形成80g溶液。
(3)t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是 c < b < a 。
(4)将t2℃时a、b、c三种物质等质量的饱和溶液降温到t1℃时,则析出的晶体的质量为它们t2℃与t1℃时的溶解度的差值(当溶剂的质量为100g时)。所以析出晶体最多的是 a。
(5)将t2℃时a、b、c三种物质等质量的饱和溶液降温到t1℃时,由于a、b的溶解度是变小的,即形成的是它们在t1℃时的饱和溶液。C物质的溶解度变大,没有晶体析出。所以C溶液的溶质质量分数与t2℃时其饱和溶液的溶质质量分数没有变化。饱和溶液的溶质的质量分数为: (注意:ab的溶解度按t1℃时计算,C的溶解度按t2℃时计算)。三物质的溶解度从大到小的顺序为:b >a> c,所以其溶液的溶质质量分数从大到小的顺序为:b >a> c。
(注意:ab的溶解度按t1℃时计算,C的溶解度按t2℃时计算)。三物质的溶解度从大到小的顺序为:b >a> c,所以其溶液的溶质质量分数从大到小的顺序为:b >a> c。
