问题
计算题
为了得到3.3mol氢气,实验室取用1000 mL某浓度盐酸(密度为1.1g/mL)与足量的锌粒完全反应。
① 盐酸含HCl的物质的量是多少?(根据化学方程式列式计算)
② 上述盐酸中HCl的质量分数为 。(保留l位小数)
答案
①设:盐酸中含HCl的量为x
Zn+2HCl→ZnCl2+H2↑
2 1
x 3.3mol
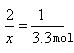 x=6.6mol
x=6.6mol
②21.9%
为了得到3.3mol氢气,实验室取用1000 mL某浓度盐酸(密度为1.1g/mL)与足量的锌粒完全反应。
① 盐酸含HCl的物质的量是多少?(根据化学方程式列式计算)
② 上述盐酸中HCl的质量分数为 。(保留l位小数)
①设:盐酸中含HCl的量为x
Zn+2HCl→ZnCl2+H2↑
2 1
x 3.3mol
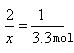 x=6.6mol
x=6.6mol
②21.9%