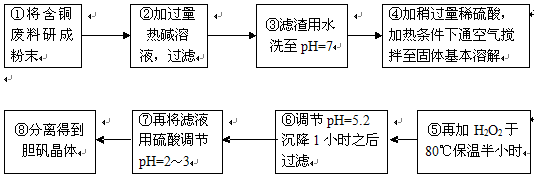
(16分)工业上需要利用一批回收的含铜废料制造胆矾(CuSO4·5H2O)。该废料中各种成份含量如下:Cu和CuO约占87%,其它为Mg、Al、Fe、Si及其氧化物,还有少量的难溶物质。工艺流程为:
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH如下表:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 | Fe(OH)2 |
| pH | 5.2 | 3.1 | 6.7 | 9.4 | 9.7 |
(1)步骤①中为什么要将含铜废料研磨成粉状?
。
(2)步骤②中的离子方程式(写出2个即可):
、 。
步骤⑤中H2O2参加反应的离子方程式: 。
(3)步骤⑥中调节溶液pH时适宜的物质是 (填序号);
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Cu(OH)2 E.MgCO3
步骤⑥中滤渣成份的化学式 。
(4)步骤⑦中用硫酸调节pH=2~3的原因是 。
步骤⑧的分离方法是 。
(16分)(1)增大固体反应物的表面积,增大化学反应的速率。(2分)
(2)2Al+2OH-+2H2O=2AlO2-+3H2↑; Si+2NaOH+H2O=Na2SiO3+2H2↑;
Al2O3+2OH-=2AlO2-+H2O; SiO2+2NaOH=Na2SiO3+H2O 。
(每写出其中1个给2分,共4分,没气体符号扣1分,未配平0分)
2Fe2++H2O2 +2H+=2Fe3++2H2O (2分)
(3)C、D (2分) Fe(OH)3 (1分)
(4)加热蒸发浓缩时会导致Cu2+发生水解生成Cu(OH)2,用硫酸调节pH=2~3是为了抑制Cu2+的水解,也不会引入杂质。 (2分) 蒸发浓缩,冷却结晶,过滤。(3分)
(1)将含铜废料研磨成粉状,可以)增大固体反应物的表面积,增大化学反应的速率。
(2)废料中能和氢氧化钠反应的是铝、硅、氧化铝和二氧化硅,所以方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑、Si+2NaOH+H2O=Na2SiO3+2H2↑、Al2O3+2OH-=2AlO2-+H2O、SiO2+2NaOH=Na2SiO3+H2O。双氧水的目的是氧化混合液中的亚铁离子,生成铁离子,以形成氢氧化铁沉淀而除去,所以方程式为2Fe2++H2O2 +2H+=2Fe3++2H2O。
(3)用于既要调节溶液的pH,又不能引入杂质,所以应该选择CD。通过控制溶液的pH以形成氢氧化铁沉淀,即步骤⑥中滤渣成份的化学式Fe(OH)3 。
(4)由于溶液中铜离子水解显酸性,加热蒸发浓缩时会导致Cu2+发生水解生成Cu(OH)2,所以用硫酸调节pH=2~3是为了抑制Cu2+的水解,且也不会引入杂质。要从溶液中分离得到硫酸铜晶体,可以通过蒸发浓缩,冷却结晶,过滤即可。
