问题
选择题
具有强氧化性的高铁酸盐(FeO42-)是公认的绿色、高效的水处理剂,其制备方法可以表示为:aFe3++bClO-+cM=dFeO42-+eCl-+fH2O,关于该反应下列说法中正确的是( )
A.M代表H+
B.FeO42-是氧化产物
C.ClO-在反应中被氧化
D.生成1mol FeO42-时共转移1.5mol电子
答案
答案:B
题目分析:利用氧化还原反应中得失电子守恒,配平化学方程式:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O。从化合价变化,可知FeO42-是氧化产物,因此选项B正确。而ClO-中氯元素的化合价降低,在反应中被还原。由方程式可知,生成2mol FeO42-时转移电子6mol,因此生成1mol FeO42-时共转移3mol电子。综上,答案选B。
点评:考查氧化还原反应的相关概念,属于基础题。在计算转移电子数时,应注意结合方程式,列比例求解。

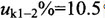 %=10.5,
%=10.5,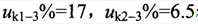 ;K1点短路时35kV母线不提供反馈电流,试求10kV母线的短路电流与下列哪一个值最接近?()
;K1点短路时35kV母线不提供反馈电流,试求10kV母线的短路电流与下列哪一个值最接近?()