问题
实验题
某同学根据题目提示和要求选择下列仪器设计实验,验证:
Zn+2H2SO4 (浓)  ZnSO4+SO2↑+2H2O;
ZnSO4+SO2↑+2H2O;
Zn+H2SO4(稀)==ZnSO4+H2↑ 提示和要求:
①供选用的试剂有:98%浓硫酸,锌粒,氧化铜,碱石灰,无水硫酸铜,溴水,品红试液,碱石灰,
②二氧化硫具有还原性,可能与金属氧化物发生还原反应;
③E和F仪器同时使用;
④仪器可以重复使用.
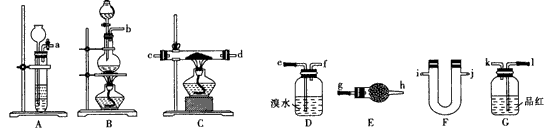
(1)组合装置(气流从左至右)的接口连接顺序:____。
(2)D装置发生反应的离子方程式:_______;C装置发生反应的化学方程式: ___________。
(3)E装置中药品是碱石灰,F装置应装入_________,其作用是________。
(4)证明锌与浓硫酸反应有二氧化硫产生的现象是_________;锌与稀硫酸反应产生氢气的现象是____________。
(5)简述锌与浓硫酸反应开始不产生氢气的原因________。
答案
(l)b→1-k→e-f→1-k→g-h→cd(dc)→ij(ji)
(2)SO2+2H2O+Br2==SO42-+2Br-+4H+; CuO+H2 Cu+H2O
Cu+H2O
(3)无水硫酸铜;检验产物水
(4)气体开始通人品红溶液时,品红褪色;C中黑色粉末变红色,F中无水硫酸铜由白色变成蓝色
(5)浓硫酸中主要以H2SO4形式存在,H+很少;且+6价硫的氧化性强于H的氧化性
