(1) 已知在一定条件下的反应4HCl+O2=2Cl2 +2H2O中, 有4mol HCl被氧化时,放出120kJ的热量,且
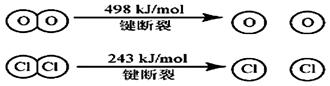
则断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差为__________KJ。
(2)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ·mol-1) | 786 | 715 | 3401 |
(3)已知AlCl3熔点190℃,沸点183℃,结构如右图所示:AlCl3晶体内含有的作用力有 (填序号)。
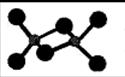
A.离子键 B.共价键 C.金属键
D.配位键 E.范德华力 F. 氢键
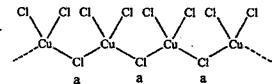
(4)氯和钾与不同价态的铜可生成两种化合物,这两种化合物中的阴离子均为无限长链结构(如下图),a位置上Cl原子的杂化轨道类型为 ,已知其中一种化合物的化学式为KCuCl3,另一种的化学式为 。
(1)33
(2)MgO> CaO> NaCl > KCl (3) B、D、E(漏一个扣1分,错选0分)
(4)SP3 K2CuCl3
题目分析:(1)△H=断裂化学键吸收的能量-形成化学键放出的能量=4×x kJ/mol+498k
J/mol-2×243kJ/mol-2×2×y kJ/mol=-120kJ/mol,解得y-x=33kJ/mol。
(2)离子半径Mg2+<Na+<O2-<Ca2+<Cl-;离子电荷数Na+=Cl-<O2-=Mg2+=Ca2+,离子晶体的离子半径越小,带电荷数越多,晶格能越大,则晶体的熔沸点越高,则NaCl、KCl、MgO、CaO熔点由高到低的顺序是MgO>CaO>NaCl>KCl。
(3)已知AlCl3熔点190℃,沸点183℃,这说明氯化铝的熔沸点很低,所以形成的晶体类型是分子晶体,根据结构可知,分子中含有的作用力有共价键、配位健和分子间作用力,答案选BDE。
(4)a位置上Cl原子成2个单键,含有2对孤对电子,杂化轨道数为4,所以杂化轨道类型为sp3。一种化合物的化学式为KCuCl3,其中铜元素为+2价,故另一种化合物中铜为+1价,CuCl3原子团的化合价为-2,其化学式为:K2CuCl3。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,在注重对学生基础知识巩固和训练的同时,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的应试能力和逻辑推理能力。
