A、B、C、D四种短周期元素,A元素有三个电子层,其中最外层电子数占总电子数的1/6;B元素原子核外电子数比A元素原子核外电子数多1;C-离子核外电子层数比A元素的离子核外电子层数多1;D元素原子最外层电子数是次外层的2倍.请填写下列空格:
(1)请写出A的元素符号______;(2)C离子的结构示意图______;
(3)A的单质能在D的最高价氧化物中燃烧,反应的方程式为______.
(4)B的最价氧化物可溶于氢氧化钠溶液写出反应的离子方程式______.
(5)C、D最高价氧化物对应的水化物酸性______ 强于______(填化学式)
可设计简单实验证明,实验步骤如下:______.
A、B、C、D四种短周期元素,A元素有三个电子层,其中最外层电子数占总电子数的
,令最外层电子数为x,则×1 6
×(10+x)=x,解得x=2,故A为镁元素;B元素原子核外电子数比A元素原子核外电子数多1,则B为铝元素;C-离子核外电子层数比A元素的离子核外电子层数多1,镁离子有2个电子层,则C-离子有3个电子层,核外电子数为18,故C为氯元素;D元素原子最外层电子数是次外层的2倍,则D有2个电子层,最外层电子数为4,则D为碳元素.1 6
(1)由上述分析可知A为Mg元素.
故答案为:Mg.
(2)氯离子质子数为17,核外电子数为18,核外有3个电子层,最外层有8个电子,氯离子结构示意图为
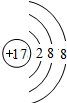
.
故答案为:

.
(3)镁在二氧化碳中燃烧生成碳和氧化镁,反应方程式为2Mg+CO2
C+2MgO. 点燃 .
故答案为:2Mg+CO2
C+2MgO. 点燃 .
(4)氧化铝与氢氧化钠溶液反应生成偏铝酸钠与水,反应离子方程式为Al2O3+2OH-═2AlO2-+H2O.或者写成
Al2O3+2OH-+3H2O=2[Al(OH)4]-.
故答案为:Al2O3+2OH-═2AlO2-+H2O(或Al2O3+2OH-+3H2O=2[Al(OH)4]-).
(5)非金属性Cl>C,所以最高价氧化物对应的水化物酸性HClO4>H2CO3.将HClO4溶液滴入Na2CO3溶液中,有无色无味使澄清石灰水便混浊的气体生成.
故答案为:HClO4;H2CO3;将HClO4溶液滴入Na2CO3溶液中,有无色无味使澄清石灰水便混浊的气体生成.
