用竖式计算.
|
(1)504×2=1008;
504
;×2 1008
(2)213×5=1065;
213
;×5 1065
(3)109×8=872;
109
;×8 872
(4)650×4=2600;
650
;×4 2600
(5)1300×9=11700;
1300
;×9 11700
(6)328×3=984;
328
.×3 984
用竖式计算.
|
(1)504×2=1008;
504
;×2 1008
(2)213×5=1065;
213
;×5 1065
(3)109×8=872;
109
;×8 872
(4)650×4=2600;
650
;×4 2600
(5)1300×9=11700;
1300
;×9 11700
(6)328×3=984;
328
.×3 984
环境问题备受世界关注.化工厂以及汽车尾气排放的一氧化碳(CO)、氮氧化物(NOx)、硫化物等气体己成为大气污染的主要因素.
(1)CO的中毒是由于CO与血液中血红蛋白的血红素部分反应生成碳氧血红蛋白,反应方程式可表示为:CO+Hb•O2

O2+Hb•CO
实验表明,c(Hb•CO)即使只有c(Hb•O2)的 1/50,也可造成人的智力损伤.
已知t℃时上述反应的平衡常数K=200,吸入肺部O2的浓度约为1.0×10-2mol•L-1,若使c(Hb•CO)小于c(Hb•O2)的 1/50,则吸入肺部CO的浓度不能超过______mol•L-1.
(2)汽车尾气治理的方法之一是在汽车的排气管上安装一个“催化转化器”.
已知反应2NO(g)+2CO(g)

N2(g)+2CO2(g)△H=-113kJ•mol-1
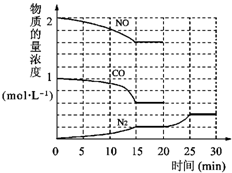
①为了模拟催化转化器的工作原理,在t℃时,将2molNO与1mol CO充入lL反应容器中,反应过程中NO(g)、CO(g)、N2(g)物质的量浓度变化如右下图所示.反应进行到15min时,NO的平均反应速率为______,
②观察在20min~30min内N2(g)发生变化的曲线图,判断引起该变化的条件可能是______;
a.加入催化剂
b.降低体系温度
c.缩小容器体积为0.5L
d.增加CO2的物质的量
(3)煤化工中常需研究不同温度下平衡常数、投料比及产率等问题.
已知:CO(g)+H2O(g)

H2(g)+CO2(g)的平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
①上述正向反应是:______反应(填“放热”、“吸热”).
②某温度下上述反应平衡时,恒容、升高温度,正反应速率______(填“增大”、“减小”或“不变”),容器内混合气体的压强______(填“增大”、“减小”或“不变”).
③在830℃发生上述反应,以下表中的物质的量投入恒容反应器,其中向正反应方向移动的有______(选填A、B、C、D).
| A | B | C | D | |
| n(CO2) | 3 | 1 | 0 | 1 |
| n(H2) | 2 | 1 | 0 | 1 |
| n(CO) | 1 | 2 | 3 | 0.5 |
| n(H2O) | 5 | 2 | 3 | 2 |
(由单选和多选组成)
ZH机械制造总厂聘请第三方咨询机构对其生产的XR牌机械产品进行全国满意度调查,此次顾客满意度专项调查由品牌形象、预期质量、感知质量、感知价值、顾客满意、顾客忠诚等六个结构变量构成测评模型。其调查问卷部分问题如表2.3-1所示。
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
你认为问卷中的第21和第22评价项是评价( )结构变量的。
A.价格敏感度
B.顾客抱怨
C.顾客满意
D.顾客忠诚