一定温度下,在2L的密闭容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,依据题意,回答下列问题.(1)反应开始到10s,用Z表示的反应速率为______;
(2)反应达到平衡时,Y的转化率为______;该反应的化学平衡常数K的表达式是______;
(3)能说明该反应已经达到平衡状态的是______;
a.生成1mol X的同时,生成2mol Z b.容器内气体的压强保持不变
c.v逆(X)=v正(Y) d.容器内气体的密度保持不变
(4)为使该反应的反应速率增大,且能使平衡向正反应方向移动的是______.
a.平衡后及时分离出Z气体 b.平衡后加入高效催化剂
c.平衡后将各物质的量同时加倍 d.平衡后仅增大X的浓度.
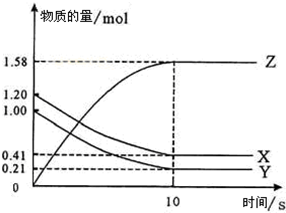
(1)由图可知10s内,Z的物质的量变化为1.58mol,故v(Z)=
=0.079mol/(L•s ).1.58mol 2L 10s
故答案为:0.079mol/(L.s );
(2)由图可知,Y的起始物质的量为1mol,平衡时Y的物质的量为0.21mol,参加反应的Y的物质的量为1mol-0.21mol=0.79mol,故Y的转化率为
×100%=79%;0.79mol 1mol
由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,10后X、Y、Z的物质的量不再变化,该反应为可逆反应,且△n(X):△n(Y):△n(Z)=(1.2-0.41)mol:(1-0.21)mol:1.58mol=1:1:2,则反应的化学方程式为:X+Y
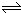
2Z,该可逆反应的平衡常数k=
.c2(Z) c(X)•c(Y)
故答案为:79%;
.c2(Z) c(X)•c(Y)
(3)a.生成1molX相当于消耗2molZ,同时生成2molZ,说明到达平衡,故a正确;
b.该反应气体的物质的量不发生变化,容器内气体的压强自始至终保持不变,压强不变不能说明到达平衡,故b错误;
c.v逆(X)=v正(Y)说明不能物质表示正逆速率之比等于化学计量数之比1:1,说明反应到达平衡,故c正确;
d.反应混合物都是气体,气体的总质量不变,容器的容积一定,容器内气体的密度自始至终保持不变,故密度保持不变不能说明反应到达平衡,故d错误.
故选:ac.
(4)a.平衡后及时分离出Z气体,瞬间逆反应速率减小,正反应速率不变,平衡向正反应进行,随后反应混合物各组分的浓度降低,速率减小,故a错误;
b.平衡后加入高效催化剂,同等程度增大正、逆反应速率,平衡不移动,故b错误;
c.平衡后将各物质的量同时加倍,反应混合物的浓度增大,反应速率增大;该反应气体的物质的量不发生变化压强增大,平衡不移动,故c错误.
d.平衡后仅增大X的浓度,瞬间正反应速率增大,逆反应速率不变,平衡向正反应进行,随后生成物的浓度增大,逆反应速速率增大,故d正确.
故选:d.