碱式碳酸铜是一种化工原料,化学式用mCu(OH)2·nCuCO3表示。实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:

Ⅰ.废铜屑制硝酸铜
方案1:将铜屑在空气中充分灼烧,残留固体溶于稀硝酸;
方案2:如图1(夹持仪器已省略)。将浓硝酸缓慢加到废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
方案3:将方案2中浓硝酸换成稀硝酸,其他不变。
Ⅱ.碱式碳酸铜的制备
①向大试管中加入碳酸钠溶液和硝酸铜溶液
②水浴加热至70 ℃左右
③用0.4 mol·L-1的NaOH溶液调节pH至8.5,振荡、静置、过滤
④用热水洗涤、烘干,得到碱式碳酸铜产品
请回答下列问题:
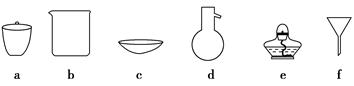
(1)按方案1实验,必须选择的下列仪器有________(填序号)。
(2)图2中能分别替代图1中B和C装置的是________(填装置序号)。
(3)已知:NO+NO2+2NaOH===2NaNO2+H2O;2NO2+2NaOH===NaNO3+NaNO2+H2O,NO不能单独与NaOH溶液反应,实验结束时,如何操作才能使装置中的有毒气体被NaOH溶液完全吸收?__________________________。
(4)步骤④中洗涤的目的是______________________________________。
(5)步骤③过滤后的滤液中含有CO32—,检验CO32—的方法是_________________________________________________________。
(6)测定碱式碳酸铜组成的方法主要有两种:
方法1 灼烧法:取34.6 g纯净物mCu(OH)2·nCuCO3,在硬质试管里灼烧,将气体产物依次通入足量的浓硫酸、足量的碱石灰中,完全吸收后浓硫酸净增1.8 g,碱石灰净增8.8 g。
方法2 还原法:在氢气中加强热,测反应前后固体的质量。
①利用上述数据推算碱式碳酸铜的化学式_____________________。
②配平化学方程式:mCu(OH)2·nCuCO3+________H2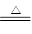 ________Cu+________CO2↑+________H2O
________Cu+________CO2↑+________H2O
(1)abe (2)Ⅰ、Ⅱ和Ⅲ (3)关闭活塞b,打开活塞a,通入一段时间空气 (4)除去产品表面杂质 (5)取少量滤液于试管中,加入稀盐酸,将产生的气体通入澄清石灰水中,溶液变浑浊,说明滤液中含有CO32—
(6)①Cu(OH)2·2CuCO3 ②(m+n) (m+n)
n (2m+n)
(1)灼烧固体需要的仪器有坩埚、三脚架、泥三角、玻璃棒、酒精灯;溶解固体需要的仪器有烧杯、玻璃棒。(2)B用作安全瓶,C用于吸收氮的氧化物,替代B和C的装置必须具有吸收氮的氧化物和防倒吸双重功能。Ⅰ、Ⅱ装置能防倒吸,Ⅲ装置烧杯中的下层液体为四氯化碳,氮的氧化物不溶于四氯化碳,不会导致装置内的气压急剧减小,当氮的氧化物从四氯化碳层进入烧碱溶液中,被氢氧化钠溶液吸收,Ⅲ装置既可以防倒吸,又能使氮的氧化物被吸收。(3)根据所给反应方程式知,通入足量的空气,使一氧化氮转化成二氧化氮能被完全吸收。(4)固体产品表面会吸附一些杂质,洗涤可除去碱式碳酸铜表面的杂质。(5)用盐酸和CO32—反应生成CO2,再用澄清石灰水检验二氧化碳。(6)①浓硫酸吸收生成的水,碱石灰吸收生成的二氧化碳,则:n(CO2)=8.8/44=0.2 mol,n(H2O)=1.8/18=0.1 mol。灼烧碱式碳酸铜的反应方程式为mCu(OH)2·nCuCO3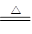 (m+n)CuO+mH2O+nCO2↑,故m/n=0.1/0.2=1/2。该碱式碳酸铜的化学式为Cu(OH)2·2CuCO3。
(m+n)CuO+mH2O+nCO2↑,故m/n=0.1/0.2=1/2。该碱式碳酸铜的化学式为Cu(OH)2·2CuCO3。
②根据题给方程式和氧原子守恒知,氧原子的计量数为(2m+3n)-2n=2m+n,即水的计量数为2m+n,由水的计量数推知氢分子的计量数: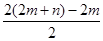 =m+n,则化学方程式为mCu(OH)2·nCuCO3+(m+n)H2
=m+n,则化学方程式为mCu(OH)2·nCuCO3+(m+n)H2 (m+n)Cu+nCO2↑+(2m+n)H2O。
(m+n)Cu+nCO2↑+(2m+n)H2O。
