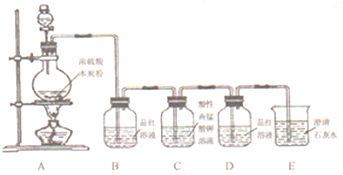
某学生用如图装置来做浓硫酸和木炭反应的实验:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,以及检验生成的CO2和SO2气体.△ .
回答下列问题:
(1)装置B中观察到的现象是______,可确定该气体中含有______.
(2)装置C中酸性KMnO4溶液用于除去SO2,是利用了SO2具有______(填“氧化性”或“还原性”),其目的是______(填“甲”或“乙”)
甲:防止SO2干扰CO2的检验乙:可吸收CO2气体
(3)装置D中品红溶液不褪色,可证明SO2______(填“已除尽”或“未除尽”).
(4)装置E中观察到的现象是______,可确定该气体中含______,反应的化学方程式为______.
(5)若用6g木炭和足量的浓硫酸反应,能收集到标准状况下CO2______L.(相对原子质量:C-12)
(1)反应C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O中生成二氧化硫气体,所以装置B中品红溶液褪色,证明生成的气体中含有SO2,△ .
故答案为:品红溶液褪色;SO2;
(2)装置C中酸性KMnO4溶液用于除去SO2,利用了二氧化硫的还原性,除去二氧化硫的目的是防止SO2干扰CO2的检验,所以甲正确,
故答案为:还原性;甲;
(3)装置D中品红溶液不褪色,说明装置C已经将混合气体的二氧化硫除尽,
故答案为:已除尽;
(4)装置E中为澄清石灰水,二氧化碳气体能够使澄清石灰水变浑浊,所以装置E中澄清石灰水变浑浊,由于二氧化硫已经除尽,说明混合气体中一定含有二氧化碳,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O,
故答案为:溶液变浑浊;CO2+Ca(OH)2=CaCO3↓+H2O;
(5)6gC的物质的量为:
=0.5mol,根据碳原子质量守恒可得,生成二氧化碳的物质的量为0.5mol,标准状况下0.5mol二氧化碳的体积为:22.4L/mol×0.5mol=11.2L,6g 12g/mol
故答案为:11.2L.
