问题
计算题
某工厂生产的纯碱中含有少量氯化钠杂质,产品包装袋上说明如下:
| XX纯碱 |
| 主要成分:Na2CO3 |
| Na2CO3含量≥98% |
| 作用:造纸,纺织等 |
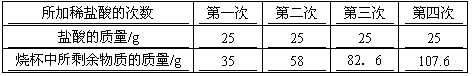
答案
(1)4.4 g
(2) 解:设12g样品中含碳酸钠的质量为x
Na2CO3+2HCl===2NaCl+H2O+CO2↑
106 44
x 4.4g
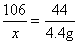 x=10.6g
x=10.6g
样品中碳酸钠的质量分数为
该纯碱产品中碳酸钠的质量分数与包装袋上说明不符。
某工厂生产的纯碱中含有少量氯化钠杂质,产品包装袋上说明如下:
| XX纯碱 |
| 主要成分:Na2CO3 |
| Na2CO3含量≥98% |
| 作用:造纸,纺织等 |

(1)4.4 g
(2) 解:设12g样品中含碳酸钠的质量为x
Na2CO3+2HCl===2NaCl+H2O+CO2↑
106 44
x 4.4g
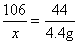 x=10.6g
x=10.6g
样品中碳酸钠的质量分数为
该纯碱产品中碳酸钠的质量分数与包装袋上说明不符。