问题
计算题
实验室用6.5g锌与100g稀硫酸反应,当恰好完全反应时,求:
(1)可制得氢气的质量是多少?(2)该硫酸溶液的溶质质量分数。
答案
解:设可制的氢气的质量为X,需要硫酸的质量为Y
(1)由题意可知锌完全反应
Zn + H2SO4==ZnSO4 + H2↑
65 98 2
6.5g Y X
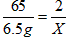 X=0.2g
X=0.2g
(2)需要硫酸的质量:
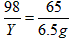 Y=9.8g
Y=9.8g
硫酸溶液的质量分数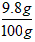 ×100%=9.8%
×100%=9.8%
答:制取氢气的质量为0.2克;硫酸溶液的质量分数为9.8%。
