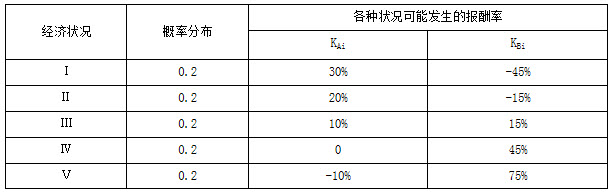
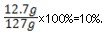问题
计算题
将5.6g铁放入121.6g稀盐酸中恰好完全反应。求:
(1)生成氢气的质量。
(2)反应后溶液中溶质的质量分数。
答案
解:设5.6g铁放入121.6g稀盐酸中生成氢气质量为X,同时生成氯化亚铁的质量为Y
则:Fe+2HCl═=FeCl2+H2↑
56 127 2
5.6g Y X
根据: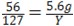 解得Y=12.7g
解得Y=12.7g
根据: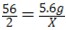 解得X=0.2g
解得X=0.2g
(1)生成氢气质量为0.2g;
(2)反应后所得溶液的质量为:5.6g+121.6g﹣0.2g=127g
所以反应后溶液中溶质的质量分数为: