为测定石灰石样品的纯度(样品中的杂质既不溶于水也不与盐酸反应,且耐高温).取10g该石灰石样品,再把100g盐酸平均分 4次加入样品中,充分反应后剩余固体的质量见下表:

求:
(1)石灰石样品的纯度;
(2)所用盐酸的质量分数;
(3)100g这种纯度的石灰石跟一定量的盐酸恰好完全反应后,溶液中溶质的质量分数.
(1)石灰石样品中CaCO3的质量分数为: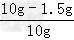 ×100%=85%
×100%=85%
(2)解:由题意知:第一次25g稀盐酸恰好反应掉10g﹣6.575g=3.425g碳酸钙.
设第一次实验中,所加入的10g盐酸中溶质的质量为X
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
3.425g x
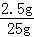
x=2.5g
所用稀盐酸中溶质的质量分数=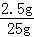 ×100%=10%
×100%=10%
(3)100g石灰石中碳酸钙的质量是100g×85%=85g.
设参加反应的盐酸溶质的质量为y,生成氯化钙的质量是z,生成二氧化碳的质量是m.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 111 44
85g y z m
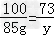
y=62.05g
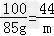 z=94.35g
z=94.35g
m=37.4g
所以所用盐酸的质量是62.05g÷10%=620.5g,根据质量守恒定律可知氯化钙溶液的质量是85g+620.5g﹣37.4g=668.1g.所以氯化钙溶液溶质的质量分数= 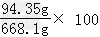 %≈14.1%
%≈14.1%
答:石灰石样品的纯度是85%,所用盐酸的质量分数是10%,完全反应后溶液中溶质的质量分数是14.1%
