问题
填空题
高铁酸钾(K2FeO4)是新型多功能水处理剂,碱性条件下性质稳定,其生产过程如下:
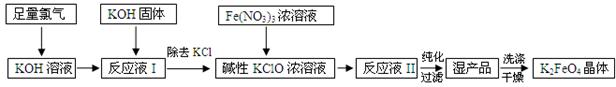
请回答下列问题
(1)氯碱工业制Cl2的化学反应方程式 ;
(2)生成“反应液Ⅱ”的离子方程式是 ;(3)使用碱性KClO的原因是 ;
(4)从“反应液II”中分离出K2FeO4后 ,副产品是KCl和 (填化学式),该混合物可用 方法分离提纯(填字母序号);
A.过滤
B.分液
C.蒸馏
D.重结晶(5)工业生产3.96t K2FeO4,理论上消耗Cl2的物质的量为______mol。
答案
(1)2NaCl + 2H2O 2NaOH + H2↑+ Cl2↑
2NaOH + H2↑+ Cl2↑
(2)3ClO- + 2Fe3+ + 10OH- = 2FeO42- + 3Cl- + 5H2O;
(3)K2FeO4在碱性条件下稳定;KClO氧化性强于K2FeO4
(4) KNO3 ; D
(5) 3.00 × 104
题目分析:(1)氯碱工业就是电解饱和食盐水得到烧碱和氯气;(2)根据流程分析反应液II是利用次氯酸钾氧化铁离子得到FeO42-,结合氧化还原反应离子方程式的书写步骤可得:3ClO- + 2Fe3+ + 10OH- = 2FeO42- + 3Cl- + 5H2O;(3)题目信息:K2FeO4在碱性条件下稳定,反应需在碱性条件下进行;(4)反应中加入了硝酸铁,所以还生成KNO3,硝酸钾的溶解度随温度变化较大,可以用冷却结晶的方法分离;(5)根据氯气与碱反应和次氯酸钾与硝酸铁反应的关系式进行计算。
