实验探究活动中,小明进行如下实验:
(1)打开两瓶溶质质量分数均为l 0%的盐酸和硫酸,观察到其中一个试剂瓶瓶口有白雾现象,该试剂瓶盛装的试剂是______;将湿润的蓝色石蕊试纸靠近白雾,将观察到______.
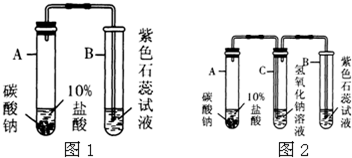
(2)小明设计了图1装置(固定装置已略去)验证CO2能否与水反应,并认为:如果观察到紫色石蕊试液变红,说明CO2能与水反应并生成酸性物质.
①写出试管A中反应的化学方程式:______.
②老师指出:虽然CO2不是酸性物质,但也不能根据石蕊试液变红的现象说明CO2能与水反应并生成酸性物质.为什么?答:______.
③根据老师的提示,小明对实验作如下两种改进:
方案甲:仍用原装置,但用硫酸替代盐酸进行实验.
方案乙:对装置作如图2所示的改进.
上述两种改进方案中,可行的是方案______ (填“甲”或“乙”),另一种改进方案不可行的原因是______.
(1)盐酸具有挥发性,打开瓶塞会看到白雾,是挥发出的氯化氢气体溶于水形成的盐酸小液滴,所以打开两瓶溶质质量分数均为l 0%的盐酸和硫酸,观察到其中一个试剂瓶瓶口有白雾现象,说明该瓶所转试剂是l 0%的盐酸;该白雾显酸性,可使蓝色石蕊试纸变红;
(2)①试管A中碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,方程式是:2HCl+Na2CO3═2NaCl+CO2↑+H2O;
②盐酸挥发的氯化氢气体溶于水显酸性,也能使石蕊试液变红,所以该推理是不严密的;
③要检验CO2能与水反应并生成酸性物质,须排除氯化氢气体的干扰,方案甲用硫酸是可行的;方案乙,用氢氧化钠溶液不仅吸收HCl,而且也能吸收CO2,所以是不可行的;
故答案为:(1)10%盐酸(或盐酸); 试纸变红;
(2)①2HCl+Na2CO3═2NaCl+CO2↑+H2O;
②紫色石蕊试液遇HCl也能变红色;
③甲;氢氧化钠溶液不仅吸收HCl,而且也能吸收CO2.

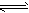 2AB(g)达到平衡状态的标志是 [ ]
2AB(g)达到平衡状态的标志是 [ ]