问题
选择题
5.6g含一种杂质的不纯的铁和足量的稀盐酸反应放出0.21g氢气,则铁片中含有的另一种金属杂质是下列金属中的①Zn ②Mg ③Cu ④Al( )
A.①或②
B.②或③
C.③或④
D.②或④
答案
设该混合物为纯净单质金属M(化合物中化合价统一为+2价)反应,其相对原子质量为x.
M+2HCl=MCl2+H2↑
x 2
5.6g 0.21g
=x 5.6g 2 0.21g
x≈53.3由于铁的相对原子质量为56,所以既然混合物的相对原子质量为53.3,所以含杂质的相对原子质量一定小于53.3,符合题意的有镁和铝.锌大于56,所以不会含有.铜不反应,更不会含有.铝为三价金属,相对原子质量为27,当理解为+2价,可以看成是相对原子质量为18.
故选D.

 ,传送带以
,传送带以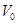 =10m/s 的速率逆时针转动.在传送带上端A无初速地放一个质量为m=0.5kg的黑色煤块,它与传送带之间的动摩擦因数为μ=0.5.煤块在传送带上经过会留下黑色划痕 已知sin37o=0.6,g=10
=10m/s 的速率逆时针转动.在传送带上端A无初速地放一个质量为m=0.5kg的黑色煤块,它与传送带之间的动摩擦因数为μ=0.5.煤块在传送带上经过会留下黑色划痕 已知sin37o=0.6,g=10 ,(1)求煤块从A到B的时间。(2)煤块从A到B的过程中传送带上形成划痕的长度。
,(1)求煤块从A到B的时间。(2)煤块从A到B的过程中传送带上形成划痕的长度。