某校兴趣小组用如图Ⅰ装置制取漂白液(气密性已检验,试剂已添加),并研究其相关性质。
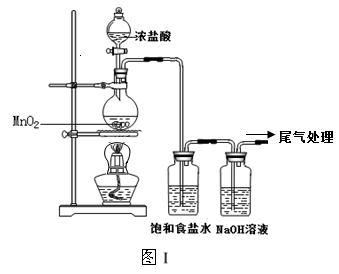
实验操作和现象:打开分液漏斗的活塞,缓缓滴加一定量浓盐酸,点燃酒精灯;一段时间后,关闭分液漏斗的活塞,熄灭酒精灯。
(1)烧瓶中反应的化学方程式是 。
(2)饱和食盐水的作用是 。
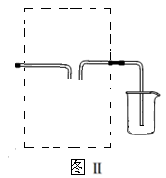
(3)若用图Ⅱ装置收集多余的氯气,请在虚线框内画出该装置简图。
(4)该小组同学用上述装置制得的漂白液中NaClO的浓度偏低。
查阅资料:在溶液中发生反应:
(a)Cl2(g)+2NaOH(aq)═ NaCl(aq)+NaClO(aq)+H2O(l)H1=-101.1kJ/mol
(b)3NaClO(aq)═2NaCl(aq)+NaClO3(aq)H2=-112.2kJ/mol
反应(a)的反应速率很快,反应(b)在室温下较慢
根据资料,请对图Ⅰ装置提出改进建议: 。
(5)修改方案后,该小组同学制得了较高浓度的NaClO溶液。他们把漂白液和滴有酚酞的红色Na2SO3溶液混合后,得到无色溶液。
提出猜想:ⅰ.NaClO把Na2SO3氧化了
ⅱ.NaClO把酚酞氧化了
ⅲ.NaClO把Na2SO3和酚酞均氧化了
①下列实验方案中可以证明NaClO氧化了Na2SO3的是 。
a.向混合后的溶液中加入过量盐酸
b.向混合后的溶液中加入过量盐酸,再加入氯化钡溶液
c.向混合后的溶液中加入过量硝酸,再加入硝酸银溶液
d.向混合后的溶液中加入氢氧化钡溶液,再加入过量盐酸
②为证明NaClO氧化了酚酞,可进行的实验是 。
(1)MnO2+4HCl(浓) 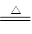 MnCl2+Cl2↑+2H2O(2)除去氯气中的氯化氢
MnCl2+Cl2↑+2H2O(2)除去氯气中的氯化氢
(3) (4)将盛NaOH溶液的洗气瓶浸在冰水中 (5)①b d ②向混合后的溶液中加入NaOH溶液,若溶液不变红说明酚酞已经被氧化;若溶液变红说明酚酞没有被氧化。
(4)将盛NaOH溶液的洗气瓶浸在冰水中 (5)①b d ②向混合后的溶液中加入NaOH溶液,若溶液不变红说明酚酞已经被氧化;若溶液变红说明酚酞没有被氧化。
题目分析:(1)烧瓶中反应的化学方程式是MnO2+4HCl(浓) 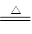 MnCl2+Cl2↑+2H2O,注意:①要写有加热符号;②必须为浓盐酸。(2)饱和食盐水的作用是除去氯气中混有的氯化氢气体;饱和氯化钠溶液可以降低氯气的溶解度;饱和氯化钠溶液可吸收氯化氢气体。(4)温度降低可以促进次氯酸钠的生成,所以我们可以将装置浸泡在冰水里。(5)只要能检验出硫酸根离子的存在,就可以证明NaClO氧化了Na2SO3。检验硫酸根离子办法:向混合后的溶液中加入过量盐酸,再加入氯化钡溶液,如果产生白色沉淀就能证明硫酸根离子的存在;向混合后的溶液中加入氢氧化钡溶液,再加入过量盐酸,如果还能生成白色沉淀就证明硫酸根离子的存在。②为证明NaClO氧化了酚酞,只要向混合后的溶液中加入NaOH溶液,若溶液不变红说明酚酞已经被氧化;若溶液变红说明酚酞没有被氧化。
MnCl2+Cl2↑+2H2O,注意:①要写有加热符号;②必须为浓盐酸。(2)饱和食盐水的作用是除去氯气中混有的氯化氢气体;饱和氯化钠溶液可以降低氯气的溶解度;饱和氯化钠溶液可吸收氯化氢气体。(4)温度降低可以促进次氯酸钠的生成,所以我们可以将装置浸泡在冰水里。(5)只要能检验出硫酸根离子的存在,就可以证明NaClO氧化了Na2SO3。检验硫酸根离子办法:向混合后的溶液中加入过量盐酸,再加入氯化钡溶液,如果产生白色沉淀就能证明硫酸根离子的存在;向混合后的溶液中加入氢氧化钡溶液,再加入过量盐酸,如果还能生成白色沉淀就证明硫酸根离子的存在。②为证明NaClO氧化了酚酞,只要向混合后的溶液中加入NaOH溶液,若溶液不变红说明酚酞已经被氧化;若溶液变红说明酚酞没有被氧化。
