问题
问答题
有一石灰石样品,其中含有的杂质为二氧化硅(二氧化硅不溶于水,也不与酸反应).取2.0g该样品,将20.0g稀盐酸平均分成4份,分4次加入到样品中,充分反应后测定剩余固体的质量,数据见下表.
| 次数 | 1 | 2 | 3 | 4 |
| 加入盐酸质量/g | 5.0 | 5.0 | 5.0 | 5.0 |
| 剩余固体质量/g | 1.3 | 0.6 | 0.2 | 0.2 |
(1)2.0g石灰石样品中杂质的质量;
(2)石灰石样品中碳酸钙的质量分数;
(3)100g这种石灰石跟足量盐酸反应,生成二氧化碳的质量.
答案
(1)由表中的数据可知第一次到第二次加盐酸可知5g盐酸能消耗0.7g碳酸钙,所以到第三次第四次所剩余的0.2g固体即是样品中的杂质为0.2g;
(2)由于样品中的杂质质量是0.2g,所以石灰石样品中碳酸钙的质量分数为
×100%=90%;、2.0g-0.2g 2.0g
(3)100g这种石灰石中含有的碳酸钙质量是100g×90%=90g;
设100g这种石灰石跟足量盐酸反应,生成二氧化碳的质量是x.
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
90g x
=100 44 90g x
x=39.6g
答:(1)2.0g石灰石样品中杂质的质量是0.2克;(2)石灰石样品中碳酸钙的质量分数为90%;(3)100g这种石灰石跟足量盐酸反应,生成二氧化碳的质量是39.6g.

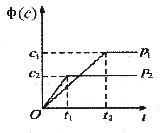
 ,生成物C的体积分数(φ)与压强p1和p2、时间t1和t2的关系如下图所示,则下列关系正确的是()。
,生成物C的体积分数(φ)与压强p1和p2、时间t1和t2的关系如下图所示,则下列关系正确的是()。