无水FeCl3呈棕红色,极易潮解,100℃左右时升华,工业上常用作有机合成催化剂。实验室可用下列装置(夹持仪器略去)制备并收集无水FeCl3。

(1)装置A中反应的离子方程式为______________________。
(2)装置F中所加的试剂为________。
(3)导管b的作用为________;装置B的作用为___________。
(4)实验时应先点燃A处的酒精灯,反应一会儿后,再点燃D处的酒精灯,原因为____________________________________。
(5)反应结束后,拆卸装置前,必须进行的操作是__________。
(6)为检验所得产品中是否含有FeCl2,可进行如下实验:取E中收集的产物少许,加水溶解,向所得溶液中加入一种试剂,该试剂为________(填序号)。
①Fe粉 ②KSCN溶液 ③酸性KMnO4溶液 ④NaOH溶液
(1)MnO2+4H++2Cl-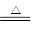 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)浓硫酸(或浓H2SO4)
(3)平衡压强(或使浓盐酸顺利流下)
除去Cl2中的HCl气体,判断实验过程中导管是否被产品堵塞
(4)排尽实验装置中的空气
(5)打开活塞a,通入空气把装置内残留的Cl2排出,保证吸收更彻底(其他合理答案均可)
(6)③
(2)FeCl3极易潮解,所以F中盛放的是浓硫酸。(3)当烧瓶中产生大量气体时压强增大,分液漏斗中的液体可能无法滴下,而导管b将烧瓶和分液漏斗上端连接,使压强相同液体便能顺利滴下;装置B盛放饱和食盐水除去Cl2中的HCl气体,若装置中有堵塞,体系的压强增大,长颈漏斗中的液面就会上升。(4)若先点燃D处酒精灯,铁丝会与装置中的空气反应,所以先点燃A处酒精灯的作用是利用生成的氯气排装置中的空气。(5)因氯气有毒拆装置前必须进行尾气吸收。(6) FeCl2具有还原性,若含有可使强氧化性的酸性KMnO4溶液褪色。
点拨:本题考查化学实验,考查考生分析化学实验现象的能力。难度中等。
