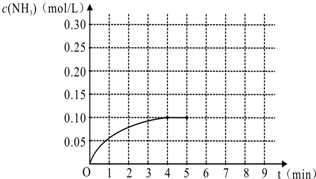
在一容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)⇌2NH3(g)△H<0,反应中NH3的物质的量浓度的变化情况如图:
(1)该反应的化学平衡常数表达式为______;
(2)根据上图,计算从反应开始到平衡时,平均反应速率v(H2)为______.
(3)判断该反应达到平衡状态的标志是______(填字母);
a.N2和NH3浓度相等 b.NH3百分含量保持不变
c.容器中气体的压强不变 d.NH3的生成速率与H2的消耗速率相等
e.容器中混合气体的密度保持不变
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为______.
a.0.20mol/L b.0.12mol/Lc.0.10mol/L d.0.08mol/L.
(1)平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,应为K=故答案为:K=
;故答案为:[NH3]2 [N2][H2]3
;[NH3]2 [N2][H2]3
(2)根据图象分析平衡时氨气的浓度为0.1mol/L,时间为4min,所以依据速率之比等于系数之比得到:v(H2)=
v(NH3)=3 2
×3 2
=0.0375 mol/(L•min),故答案为:0.0375 mol/(L•min);0.1mol/L 4min
(3)a.N2和NH3浓度相等,不能作为判断是否达到平衡的依据,二者浓度关系取决于起始量和反应的程度的关系,故不正确;
b.NH3百分含量保持不变,说明达到平衡状态,故正确;
c.容器中气体的压强不变,说明达到平衡状态,注意如果反应前后的气体的计量数之和相等时,不能作为判断的依据;
d.NH3的生成速率与H2的消耗速率相等时不能说明达到平衡状态,如是NH3的生成速率与H2的生成速率为2:3时可说明达到平衡状态;
e.容器中混合气体的密度保持不变不能作为判断的依据,因为容器的体积不变,气体的质量不变,无论是否达到平衡状态,气体的密度都不变.
故答案为:b、c;
(4)该反应为可逆反应,反应物不可能完全转化,则NH3的物质的量浓度不可能为0.2mol/L,温度改变平衡一定发生移动,则NH3的物质的量浓度不可能为0.1mol/L,故答案为:a、c;