(8分)实验室可用NH4HCO3和NaCl为原料制备纯碱。请根据下表数据和实验步骤,回答下列问题: 30℃时几种盐的溶解度/g
| NaCl | NH4HCO3 | NaHCO3 | NH4Cl | Na2SO4 | (NH4)2SO4 | CaCl2 | MgCl2 | CaSO4 |
| 36.3 | 27.0 | 11.1 | 41.4 | 40.8 | 78 | 51.7 | 26.2 | 0.165 |
①配制50 mL约25%的粗食盐水溶液(密度近似为1 g/mL)。
②精制食盐水(粗食盐中含有少量Ca2+、Mg2+、SO42-等杂质),用盐酸将滤液的pH值调至7。
③加热食盐水,将溶液温度控制在30 ─ 35℃。
④在不断搅拌下,分次将研细的NH4HCO3加入食盐水中,加完料后,继续保温、搅拌半小时。
⑤静置,趁热过滤,回收母液。晶体用蒸馏水洗涤两次。
⑥将晶体灼烧,得到纯碱。
(1)步骤①中,配制溶液的最后一步操作是 ;
(2)步骤②中,SO42-是否需要加入某种试剂除去? ,理由是
(3)步骤④中所有操作的共同目的是 ;
(4)步骤⑤中晶体的洗涤液中主要含有的杂质阳离子是 ,在通常情况下,检验这种阳离子的实验操作为 。
(1)用玻璃棒搅拌(1分)
(2)不需要(1分);除去Ca2+、Mg2+后,在溶液所控制的温度下,可能存在的硫酸盐的溶解度比NaHCO3大,且SO42-含量少,过滤后会留在母液中(2分)
(3)使生成NaHCO3的反应充分进行(1分)
(4)NH4+(1分);取少量待检物放入试管里,加入NaOH溶液,加热,将润湿的红色石蕊试纸放在管口,观察试纸是否变蓝(2分)
(1)由于是配制50 mL约25%的粗食盐水溶液,所以不需要容量瓶,因此最后一步是用玻璃棒搅拌溶液。
(2)由于除去Ca2+、Mg2+后,在溶液所控制的温度下,可能存在的硫酸盐的溶解度比NaHCO3大,且SO42-含量少,过滤后会留在母液中,所以不需要除去SO42-。
(3)步骤④的目的是制取碳酸氢钠的,所以步骤④中所有操作的共同目的是使生成NaHCO3的反应充分进行。
(4)溶液中的阳离子除了钠离子外,还主要含有NH4+,所以洗涤液中主要含有的杂质阳离子是NH4+。检验方法是取少量待检物放入试管里,加入NaOH溶液,加热,将润湿的红色石蕊试纸放在管口,观察试纸是否变蓝。

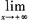 f(x)=0时,必有
f(x)=0时,必有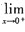 f(x)=0时,必有
f(x)=0时,必有