黄铁矿(主要成分为FeS2)是我国大多数硫酸厂制取硫酸的主要原料。某化学学习小组对某黄铁矿石进行如下实验探究。
[实验一]测定硫元素的含量。
Ⅰ、将m1 g该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
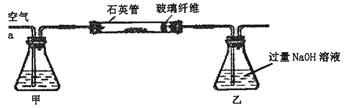
Ⅱ、反应结束后,将乙瓶中的溶液进行如下处理:
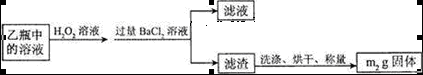
|

问题讨论:
(1)I中,甲瓶内所盛试剂是____溶液。乙瓶内发生反应的离子方程式为____。
(2)II中,乙瓶加入H2O2溶液时反应的离子方程式为_____________________。
(3)该黄铁矿中硫元素的质量分数为_______________________。
(4)III的步骤③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有____________________________________________。
(5)III的步骤④中,表示滴定已达终点的现象是
(6)Ⅲ的步骤④进行了三次平行实验,测得消耗KMnO4溶液体积分别为24.98mL、24.80mL、25.02mL(KMnO4被还原为Mn2+)。根据上述数据,可计算出该黄铁矿样品铁元素的质量分数为 。
(1)氢氧化钠(或氢氧化钾)(2分) SO2+2OH—=SO32—+H2O;(2SO32—+O2=2SO42—未写不扣分)(2分)
(2)SO32—+H2O2=SO42—+H2O (2分)
(3)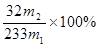 (2分)
(2分)
(4)250ml容量瓶(2分)
(5)最后一滴高锰酸钾溶液滴入时,溶液颜色突变为紫色,且在30s内不变色。(2分)
(6)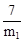 或
或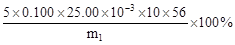 或其它合理答案(2分)
或其它合理答案(2分)
题目分析:(1)为防止SO2进入到甲装置中,可用氢氧化钠(或氢氧化钾)吸收,乙瓶中的氢氧化钠吸收硬质玻璃管中产生的二氧化硫,发生反应的离子方程式为:SO2+2OH—=SO32—+H2O,由于锥形瓶中也存在着未完全反应的氧气,故也发生2SO32—+O2=2SO42—(2)II中,乙瓶加入H2O2溶液时反应的离子方程式为SO32—+H2O2=SO42—+H2O;(3)乙瓶中的溶液产生SO42—,SO42—与加入的氯化钡中的Ba2+沉淀相结合发生沉淀反应:SO42—+Ba2+=BaSO4↓,即固体m2g为BaSO4,结合题意列关系式如下:
FeS2—2SO42——2BaSO4
1mol 2mol
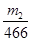
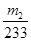
由此可知,硫元素在FeS2中的物质的量为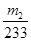 ,则其质量为:
,则其质量为: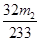 ,所以该黄铁矿中硫元素的质量分数为
,所以该黄铁矿中硫元素的质量分数为
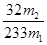 ×﹪;(4)应为250ml容量瓶;(5)因为未加入KMnO4溶液之前,溶液中含有Fe2+,溶液为浅绿色,
×﹪;(4)应为250ml容量瓶;(5)因为未加入KMnO4溶液之前,溶液中含有Fe2+,溶液为浅绿色,
当加入最后一滴高锰酸钾溶液滴入时,溶液颜色突变为紫色,且在30s内不变色,则证明到达滴定终点。
(6)发生反应的化学方程式为5Fe2++8H++MnO4-=Mn2++5Fe3++4H2O,然后根据5Fe2+—MnO4-列关系式可求得
该黄铁矿样品铁元素的质量分数为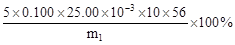 或
或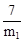
与计算。
