(14分)工业制硝酸的主要反应是4NH3(g)+5O2(g)  4NO(g)+6H2O(g)ΔH=-akJ/mol(a﹥0)
4NO(g)+6H2O(g)ΔH=-akJ/mol(a﹥0)
(1)如果将4molNH3和5molO2放入容器中,达到平衡时,放出热量0.8akJ,则反应时转移的电子数为
mol
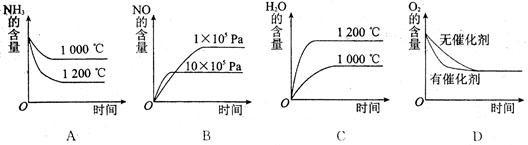
(2)若其他条件不变,下列关系图中错误的是 (选填序号)
(3)t℃时,在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如下表
| 浓度(mol/L) 时间(min) | c(NH3) | c(O2) | c(NO) | c(H2O) |
| 起 始 | 4.0 | 5.5 | 0 | 0 |
| 第2min | 3.2 | x | 0.8 | 1.2 |
| 第4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第6min | 2.0 | 3.0 | 2.0 | 3.0 |
①反应在第2mim到第4mim时,反应速率v(O2)=
②第2min时改变了条件,改变的条件可能是
A.升高温度 B.使用了催化剂 C.减小压强 D.增加了生成物
③在相同的温度下,起始向容器中加入NH3、O2、NO和H2O(g)的浓度都为1mol/L,则该反应将向 _______方向进行(填“正反应”.“逆反应”.“不移动”)
(4)工业上用水吸收二氧化氮生产硝酸,生成的NO2气体经过多次氧化、吸收的循环操作使其充分转化为硝酸(假定上述过程中无其它损失),现有23吨NO2经过2次氧化吸收得到20℅的稀硝酸 吨。
(5)成品硝酸的浓度为60%~70%,为了制浓硝酸,常用Mg(NO3)2作吸水剂,然后进行蒸馏,不用CaCl2或MgCl2作吸水剂的原因是__________________________________________
(每空2分,共14分)
(1)16
(2)AC
(3)①0.75mol.L-1.min-1 ②AB ③正反应
(4)140吨
(5) 防止生成易挥发的HCl混入HNO3中.
题目分析:
(1)根据方程式有 ,解得x=16;
,解得x=16;
(2)温度升高,平衡逆向移动,氨气的含量增加,水蒸汽含量降低,AC错;
(3)①x=4.5,v(O2)= 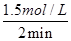 =0.75mol/(L·min);②第二个2min内,反应物的量不变,但速率加快,可能为升高温度或加入催化剂;③根据平衡常数进行计算,可以得到向正向移动。
=0.75mol/(L·min);②第二个2min内,反应物的量不变,但速率加快,可能为升高温度或加入催化剂;③根据平衡常数进行计算,可以得到向正向移动。
(4)两次氧化吸收关系为3NO2~2HNO3+NO~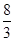 HNO3,故得到20%的硝酸140t;
HNO3,故得到20%的硝酸140t;
