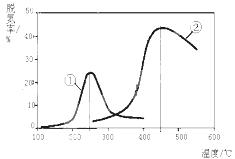
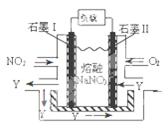
下表为四个农业区在同一年度中的粮食作物生产统计表。回答下列各题。
| 农业区 | 甲 | 乙 | 丙 | 丁 |
| 每公顷肥料使用量(公斤) | 108.8 | 53.7 | 250.8 | 191.9 |
| 每公顷收获量(公斤) | 1956 | 977 | 2495 | 3150 |
| 平均每人收获量(吨) | 121.7 | 140.6 | 6.1 | 79.2 |
| 平均每人耕地面积(公顷) | 145.6 | 186.6 | 2.1 | 37.9 |
A.机械化水平高,集约化经营
B.劳动力充足,单位面积产量高
C.人少地多,产品商品率高
D.水旱灾害频繁,水利工程量大小题2:四个农业区中最可能位于美国中部平原和我国长江中下游平原的分别是
A.甲、丙
B.甲、丁
C.乙、甲
D.乙、丁
小题1:C
小题2:A
题目分析:
小题1:从表中可以看出,乙地每公顷肥料使用量比其他地区明显少许多,每公顷收获量也是最低,说明集约化程度低;甲、乙两地突出的特点是平均每人收获量大,平均每人耕地面积大,人均产量高,产品商品率就高,所以甲、乙两农业区共同的区位条件及其生产特征是人少地多,产品商品率高;表中信息不能看出是否水旱灾害频繁。故选C。
小题2:美国中部平原有世界典型的商品谷物农业,农场规模大(平均每人耕地面积大),机械化水平高,商品率高(平均每人收获量高),集约化程度高(每公顷肥料使用量大、每公顷收获量高),应是甲;我国长江中下游平原农业历史悠久,人口周密,集约化程度高,人均耕地面积少,但单产高,应是丙。故选A。

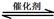 2CO2(g)+ N2(g)。△H<0
2CO2(g)+ N2(g)。△H<0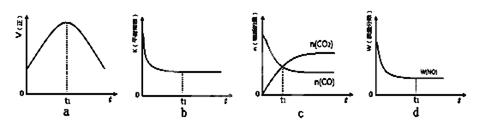
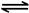 N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol 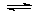 2N2(g) + 3H2O(g)。
2N2(g) + 3H2O(g)。