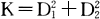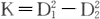问题
问答题
小王同学要想测定二块合金[甲(Cu-Zn)、乙(Cu-Ag)]中铜的质量分数,但实验室只提供一瓶标签模糊的稀盐酸和必要的仪器.根据学过的知识,(1)你认为他能测出铜的质量分数是哪一块合金?是______.(填甲或乙)理由是:______,______.
(2)现小王取该合金粉末32.5g与足量该盐酸充分反应,生成0.2mol氢气,则该合金中铜的质量为______g,该合金中铜的质量分数为______.
答案
(1)甲合金中锌在氢的前面,能与盐酸反应生成氢气,而铜不与盐酸反应生成氢气,乙中的金属都不与盐酸反应生成氢气,所以本题答案为:甲,甲中的锌在氢的前面能与盐酸反应生成氢气,而铜不与盐酸反应生成氢气Zn+2HCl═ZnCl2+H2↑,Cu+HCl不反应
(2)Zn+2HCl═ZnCl2+H2↑,
1 1
可以看出生成0.2mol氢气需要锌的物质的量为0.2mol,所以锌的质量为0.2mol×65g/mol=13g,所以铜的质量为32.5g-13g=19.5g,
该合金中铜的质量分数为
×100%=60%,所以本题答案为:19.5,60%.19.5g 32.5g