金属是我们学习的一类重要物质.
(1)下列金属制品中(如图1),利用金属导电性的是______(填字母序号).

(2)同学们在探究金属的化学性质时,做了如图2所示的两个实验(金属片已打磨).
①铁片插入硫酸铜溶液中,铁片表面的现象是______;
②铜片插入硝酸银溶液中,化学的反应方程式是______.
请结合上述两个实验,推测此实验的目的是______.
(3)某同学以铁锈为起始反应物,设计实验流程如下(部分反应条件已省略).
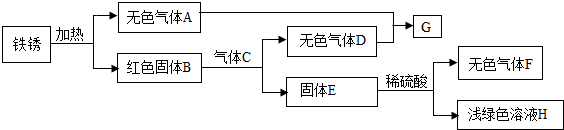
①F的化学式是______;
②B与C反应的化学方程式是______;
③A-H中,能使紫色石蕊溶液变成红色的物质是______(填化学式).
(1)不锈钢餐具是利用合金的特性一般情况下不易生锈的特点;金箔是利用金的延展性;铜导线是利用铜的导电性;
(2)①铁比铜活泼,所以铁片插入硫酸铜溶液中会置换出金属铜,同时生成硫酸亚铁,故铁片表面的现象是有红色物质析出;
②铜比银活泼,铜片插入硝酸银溶液中会置换出金属银,同时生成硝酸铜,化学的反应方程式是Cu+2AgNO3=Cu(NO3)2+2Ag;此实验的目的是比较铁、铜、银三种金属的活动性;
(3)由铁锈的成分可知,加热生成红色固体B和无色气体A,说明B是氧化铁,A是水蒸气;氧化铁和气体C反应生成固体E和无色气体D,说明C是一氧化碳,E是固体铁,而D是二氧化碳,反应的化学方程式是3CO+Fe2O3
2Fe+3CO2;二氧化碳和水反应生成碳酸,所以G就是碳酸;铁和硫酸反应生成无色气体F和浅绿色溶液H,所以F就是氢气,H就是硫酸亚铁.A-H中,能使紫色石蕊溶液变成红色的物质是二氧化碳和碳酸.高温 .
故答案为:(1)C;(2)①有红色物质析出;②Cu+2AgNO3=Cu(NO3)2+2Ag;比较铁、铜、银三种金属的活动性;(3)①H2;②3CO+Fe2O3
2Fe+3CO2;③CO2、H2CO3.高温 .
