问题
实验题
某同学欲探究赤铁矿粉(主要成分Fe2O3,杂质不反应)中Fe2O3的质量分数,他利用了如下的装置:
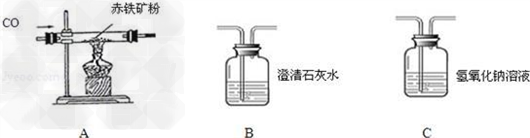
(1)写出A中发生的化学反应方程式 _________ .
(2)该装置的连接顺序为_________,B装置中可能发生的化学反应方程式是_________.
(3)实验前,测出赤铁矿粉的质量为a g; 实验完毕后,测得C装置的质量增加了w g,则该赤铁矿粉中Fe2O3的质量分数为 _________ .
(4)继续探究:若测得A装置中固体质量减少了n g,则(w﹣n)g是 _________ 的质量.
答案
(1)3CO+Fe2O3 2Fe+3CO2.
2Fe+3CO2.
(2)A、C、B;CO2+Ca(OH)2==CaCO3↓+H2O.
(3)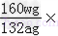 100%.
100%.
(4)一氧化碳.
