问题
填空题
(7分)元素周期表是学习物质结构和性质的重要工具,下面是元素周期表的一部分,表中所列字母A、D、E、G、Q、M、R、T分别代表某一化学元素。请用所给元素回答下列问题。
| A | |||||||||||||||||
| D | E | ||||||||||||||||
| G | Q | M | R | ||||||||||||||
| T | |||||||||||||||||
 (2)某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号) 。
(2)某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号) 。
(3)M、D两种元素形成的化合物含有的化学键类型是 ,其分子是(填“极性”或“非极性”) 分子;
A分别与D、E、R形成的分子中,分子间存在氢键的是(填分子式) 。
A与D形成分子的空间结构可能是(填序号) 。(2分)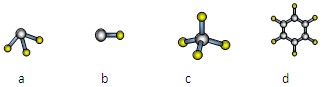
答案
(每空1分,共6分)(1) Na (2) S2- >Cl-
(3)极性共价键,非极性分子 NH3 c d (少选、错选均不给分,2分)
(1)根据元素在周期表中的位置可知,元素全部位于前四周期,所以核外电子层数是最外层电子数的3倍的元素是钠元素。
(2)Ar的原子序数为18,所以简单离子分别是S2-、Cl-。核外电子排布相同的离子,其离子半径随原子序数的增大而减小,所以离子半径是S2- >Cl-。
(3)M、D两种元素分别是S和C,形成的化合物是CS2,含有的化学键是极性键,由于是直线型结构,所以属于非极性分子。A分别与D、E、R形成的分子分别是CH4、NH3、HCl,其中含有氢键的是氨气。H和C形成的分子可以是甲烷或苯等,所以答案选cd。
