(14分)实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:
(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,
其目的是_________________________。
(2)在烧瓶中加入一定比例的乙醇和浓硫酸的混合液的方法是 。
(3)生成乙酸乙酯的反应是可逆反应,反应物不能完全转化为生成物,反应一段时间后,就达到了该反应的限度,即达到化学平衡状态。下列描述能说明该反应已达到化学平衡状态的是(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等 ⑤混合物中各物质的浓度不再变化
(4)(每空1分)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。
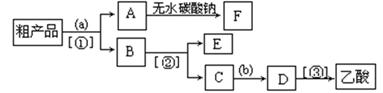
E为____________(填名称);试剂a是__________,试剂b为_______;分离方法①是___________,分离方法②是__________________,分离方法③是__________。
(5)写出C → D 反应的化学方程式 。
(1)防止烧瓶中液体暴沸
(2)先在烧瓶中加入一定量的乙醇,然后慢慢将浓硫酸加入烧瓶,边加边振荡。
(3)②④⑤
(4)(每空1分)乙醇 饱和碳酸钠溶液 浓硫酸 分液 蒸馏 蒸馏
(5)2CH3COONa + H2SO4 = Na2SO4 + 2CH3COOH
(1)酯化反应需要加热,为了防止液体沸腾时剧烈跳到,需要碎瓷片防止暴沸。
(2)浓硫酸溶于水放出大量的热,且浓硫酸的密度大于水的。为了防止乙醇和乙酸的挥发,需要把浓硫酸注入乙醇中,等冷却后,再加入乙酸。
(3)①和③中反应速率的方向是相同,在任何情况下都成立,不正确。②中反应速率的方向相反,且速率之比满足相应的化学计量数之比,正确。④⑤均符合化学平衡的特点,是正确的。答案选②④⑤
(4)粗产品中含有乙醇和乙酸,需要利用饱和碳酸钠溶液除去乙酸和乙醇,然后分液即得到乙酸乙酯溶液A,最后通过无水碳酸钠得到乙酸乙酯F。B中含有乙醇和乙酸钠以及剩余的碳酸钠。所以可直接蒸馏得到乙醇。向剩余的溶液中加入浓硫酸即得到乙酸,最后还是通过蒸馏得到乙酸。
(5)醋酸钠和硫酸反应生成醋酸和硫酸钠。
