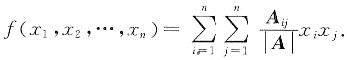图表法、图像法是常用的科学研究方法。
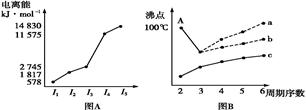
Ⅰ.图(A)是短周期某主族元素X的电离能所示情况。则X元素位于周期表的第 族。
图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第 族元素氢化物的沸点的变化规律。
Ⅱ.下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
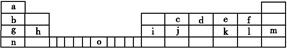
试回答下列问题:
(1)请写出元素o的外围电子排布式: 。
(2)由j原子跟c原子以1∶1相互交替结合而形成的晶体,晶体类型与晶体j相同。两者相比熔点更高的是 (填化学式),试从结构角度加以解释: 。
(3)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
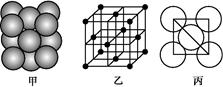
请回答:晶胞中i原子的配位数为 ,一个晶胞中i原子的数目为 ,该晶胞的空间利用率为 。
Ⅰ.ⅢA ⅣA
Ⅱ.(1)3d64s2
(2)SiC 因SiC晶体与晶体Si都是原子晶体,由于C的原子半径小,SiC中C—Si键键长比晶体Si中Si—Si键键长短,键能大,因而熔、沸点高
(3) 12 4 74%
题目分析:Ⅰ.图(A)是短周期某主族元素X的电离能所示情况。由于X的第一、第二、第三电离能相差不大,说明该元素的原子最外层有三个电子。所以X元素位于周期表的第.ⅢA。图B是研究部分元素的氢化物的沸点变化规律的图像,由于折线c表示的物质是相对分子质量越大,物质的沸点越高,符合结构相似的物质递变规律,它可以表达出第ⅣA元素氢化物的沸点的变化规律。Ⅱ.(1) o表示的是26号元素Fe。其外围电子排布式是: 3d64s2.(2)由Si原子跟C原子以1∶1相互交替结合而形成的晶体,晶体类型与晶体Si相同,都属于原子晶体。由于原子半径Si>C。原子半径越大。共价键的键长就越大,键能就越小,就越弱,断裂就容易,熔沸点更低。所以两者相比熔点更高的是SiC。(3)Al单质晶体中原子的堆积方式为面心立方堆积。在每个晶胞中与它距离相等且最近的Al原子由三个,通过每个Al原子可形成8个晶胞,由于每个Al原子都重复数了2次,所以Al原子的配位数为(3×8)÷2=12.在一个晶胞中Al原子的数目为8×1/8+6×1/2=4;假设Al原子的半径为R,则晶胞的边长L=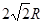 。晶胞的体积为L3=
。晶胞的体积为L3= 在一个晶胞中含有的4个Al原子的体积为
在一个晶胞中含有的4个Al原子的体积为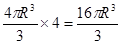 。所以该晶胞的空间利用率为(
。所以该晶胞的空间利用率为(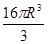 ÷
÷ )×100%=74%。
)×100%=74%。