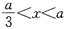A、B、C都是元素周期表中的短周期非金属元素,它们的核电荷数依次增大。A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素。D、E是第四周期元素,D原子核外最外层电子数有1个电子,其余各层电子均充满;E原子核外未成对电子数在同周期中最多。请用对应的元素符号或化学式填空:
(1)A、B、C的第一电离能由小到大的顺序为 。 A和C的氢化物沸点大小关系为 ,原因为
(2)D与E的原子化热分别为340 kJ·mol-1和400kJ·mol-1,则它们的熔点:D E(填“>”、“<”、“="”" )。
(3)分子A2B2中键与键之间的夹角为180°,并有对称性,为非极性分子,每个原子最外层电子数均满足八电子,其结构式为_____________,1mol该分子中含有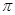 键的数目为 。
键的数目为 。
(4)基态E原子的外围电子排布式为 。EO2Cl2熔点:-96 .5℃,沸点:117℃,则固态EO2Cl2属于 晶体。
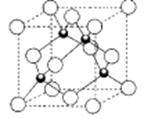
(5)D的氢化物的晶体结构如图所示,其化学式是 。
⑴C<O<N(1分) H2O>CH4 (1分) H2O分子间存在分子间氢键,且H2O为极性分子(2分)
⑵<(1分)⑶N≡C-C≡N(2分)4NA(或2.408×1024)(2分)
⑷3d54s1(1分) 分子(1分)
⑸CuH(2分)
题目分析:A原子的核外成对电子数是未成对电子数的2倍,故A的电子排布为1s22s1或1s22s22p2为Li或C;B原子的最外层p轨道的电子为半满结构,即s2p3结构,为N或P;C是地壳中含量最多的元素为O,又A、B、C都是元素周期表中的短周期非金属元素,它们的核电荷数依次增大,故ABC分别为C、N、O。D、E是第四周期元素,D原子核外最外层电子数有1个电子,其余各层电子均充满,电子排布为[Ar]3d104s1,为Cu;E原子核外未成对电子数在同周期中最多,应为3d54s1,为Cr元素;故(1)A、B、C的第一电离能由小到大的顺序为C<O<N;A和C的氢化物沸点大小关系为H2O>CH4,因为H2O分子间存在分子间氢键,且H2O为极性分子;(2)D的原子化热<E的原子化热故熔点:D <E;(3)分子A2B2中键与键之间的夹角为180°,并有对称性,为非极性分子,每个原子最外层电子数均满足八电子,其结构式为N≡C-C≡N;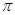 键的数目为4,故1mol该分子中含有
键的数目为4,故1mol该分子中含有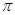 键的数目为4NA;(4)基态E原子的外围电子排布式为3d54s1;根据其性质,可知固态CrO2Cl2属于分子晶体;(5)根据晶胞结构可知含有H原子个数为4,Cu原子个数为8×1/8+6×1/2=4,故化学式为CuH。
键的数目为4NA;(4)基态E原子的外围电子排布式为3d54s1;根据其性质,可知固态CrO2Cl2属于分子晶体;(5)根据晶胞结构可知含有H原子个数为4,Cu原子个数为8×1/8+6×1/2=4,故化学式为CuH。

 (2)
(2)