问题
选择题
NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA
B.1mol Na2O2与足量H2O充分反应,转移的电子数为2NA
C.7.8g Na2O2中含有的阴离子数等于0.1NA
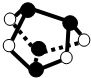
D.0.5mol雄黄(As4S4,结构如图)含有NA个S-S键
答案
A、5.6g铁粉在0.1mol氯气中充分燃烧生成氯化铁,5.6g铁粉反应需要0.15mol氯气,所以氯气不足,根据氯气计算转移的电子数,所以反应转移电子数为0.1mol×2×NAmol-1=0.2NA,故A错误;
B、过氧化钠中被氧化的O原子与被还原的O氧原子物质的量之比为1:1,所以1molNa2O2与足量H2O充分反应,转移的电子数为1mol×1×NAmol-1=NA,故B错误;
C、过氧化钠有钠离子和过氧根离子构成,7.8gNa2O2中含有的阴离子数为
×NAmol-1=NA,故C正确;7.8g 78g/mol
D、As原子原子半径比S原子大,由结构可知,黑 * * 为As原子,白 * * 为S原子,As4S4分子中不含S-S键,故D错误.
故选C.
