A.请根据下列装置图,回答有关问题:
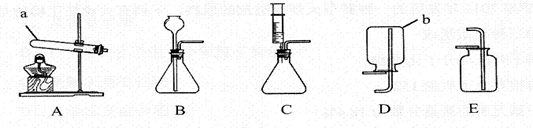
(1)写出装置图中标号仪器的名称:a :b 。
(2)写出实验室用大理石和稀盐酸反应制取二氧化碳的化学方程式 ,可选用的收集装置是 (填字母)。某同学用碳酸钠粉末和稀盐酸反应来制取二氧化碳,为了较好地控制反应速率,可选用的发生装置是 (填字母)。
B.某化学兴趣小组的学生,发现金属R不在初中学到的金属活动性顺序表中,该小组为了了解R与常见金属铝、铜的金属活动性顺序,进行如下探究活动:
【作出猜想】他们考虑到铝的活动性比铜强,对三种金属的活动性顺序作出如下猜想:
猜想一:Al>Cu>R,猜想二: ,猜想三:R> Al>Cu。
【查阅资料】 R是一种银白色的金属,在R的盐溶液中只有+2价R的盐溶液呈蓝色,常温下铝的表面会形成一层致密的氧化膜;硫酸铝、氯化铝、硝酸铝的溶液均为无色。
【实验探究】为了探究哪一种猜想成立,甲、乙、丙三位同学分别针对猜想一、猜想二、猜想三设计实验方案并展开实验探究。
| 猜想 | 主要操作 | 主要现象 | 实验结论 |
| 猜想一 | 打磨R丝,并将其插入到硫酸铜溶液中 | R丝表面覆盖了一层红色的物质 | 猜想一 (填“成立”或“不成立”) |
| 猜想二 | 打磨粗细相同的R丝、铝丝、铜丝,分别将它们插入到体积相同、溶质质量分数也相同的稀硫酸中 | ①R丝表面产生气泡缓慢,溶液由无色逐渐变成蓝色 ②铝丝表面产生气泡较快 ③铜丝表面没有气泡产生 | 猜想二成立。 R与稀硫酸反应的化学方程式为
|
| 猜想三 | 无明显现象 | 猜想三成立 |
【交流反思】
究竟哪种猜想成立?三位同学经讨论交流,发现丙同学在实验前没有打磨铝丝,这可能会导致实验结论错误。于是他们先打磨铝丝,再将其插入到丙同学做实验用过的溶液中,一段时间后,溶液的颜色 ;进而确认猜想三不成立,猜想二成立。
A.(1)试管集气瓶 (2)CaCO3 + 2HCl=CaCl2 + H2O+ CO2↑ E C B.【作出猜想】Al>R>Cu (或Cu<R<Al) 【实验探究】不成立;R+H2SO4=RSO4+H2↑ 将铝丝插入到RSO4[或RCl2或R(NO3)2]溶液中【交流反思】变浅或颜色逐渐退去
题目分析:根据仪器的形状和用途确定仪器的名称;大理石的主要成分是碳酸钙,它与稀盐酸反应生成氯化钙、水和二氧化碳,根据这些信息书写化学方程式;由于二氧化碳的密度比空气大,所以应选择向上排空气法E进行收集;要控制反应速率,需要选择装置C,通过控制注射器的快慢来控制反应速率; R、Cu、Al三种金属活动性的猜想有Al>Cu>R,R>Al>Cu,Al>R>Cu三种情况;根据R能把硫酸铜中的铜置换出来的事实可知,R的活动性比铜强,故猜想一是不成立的;由于在化合物中R的化合价是+2,所以R与稀硫酸反应的化学议程式是R+H2SO4=RSO4+H2↑;通过前面的实验已经知道Al和R的活动性都比氢强,铜的活动性比氢弱,要证明猜想三成立,只需设计实验比较R与Al的活动性强弱,根据实验现象可知是将铝丝插入到R的盐溶液中;根据猜想二的实验可知,铝的活动性比R强,且铝的盐溶液是无色的,所以将打磨后的铝丝放到R的盐溶液中可看到溶液蓝色变浅或颜色逐渐退去的现象。