下图所示的是实验室常用的实验装置.
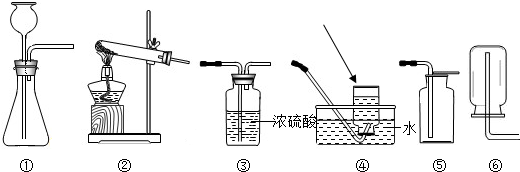
(1)图中所示仪器中,箭头所示名称为______.
(2)加热氯酸钾和二氧化锰固体制取氧气,反应中二氧化锰起______作用,反应的化学反应式为______.其发生装置为______(填序号,下同),收集装置可以选取______.
(3)此实验包括以下操作:①加热;②收集气体;③检查气密性;④装入高锰酸钾;
⑤将导管从水中移出;⑥熄灭酒精灯.正确的操作顺序是______(填序号)
(4)如果选用过氧化氢和二氧化锰制取氧气,优点是______;
A生成物只有氧气;B不需要加热;C需要加热;D原料易得
(5)研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需的时间.
| 浓度 时间(min) 条件 | 30%H2O2 | 15%H2O2 | 5%H2O2 |
| 加入agMnO2 | 0.2 | 0.8 | 2.0 |
| 加入agFe2O3 | 7.0 | 9.0 | 16.0 |
(6)如何证明制取的气体是否为氧气?
(1)从图中可看出,所示仪器中,箭头所示名称为集气瓶;
(2)加热氯酸钾和二氧化锰固体制取氧气,二氧化锰能加快氯酸钾分解产生氧气的速率,而本身的质量和化学性质都没有改变,所以二氧化锰在此反应中作催化剂,;实验室用高锰酸钾制取氧气,是固固加热型,选择②;收集氧气可用排水法或向上排空气法,故选择④或⑤;
(3)用高锰酸钾制氧气的步骤主要有七步:
①连接仪器并检查装置气密性(查);②将高锰酸钾装入大试管(装);③塞上橡皮塞并将大试管固定在铁架台上,注意要在试管口放一团棉花,试管口要略向下倾斜(定);④点燃酒精灯给试管加热,要先均匀加热,再集中在药品下部加热(点);⑤用排水集气法收集氧气,刚出来的气体是膨胀的空气,不要收,要等到有连续气泡放出时再收集(收);⑥将导气管从水槽中撤离(离);⑦熄灭酒精,停止加热(熄).注意最后两步不能颠倒;
(4)高锰酸钾在加热条件下分解制得氧气,过氧化氢和二氧化锰在常下分解制取氧气,因此选用过氧化氢和二氧化锰制取氧气较好些,不需要进行加热,操作简单,反应速度便于控制等优点;
(5)从图表数据可以看出过氧化氢相同时,催化剂的效果不同;催化剂相同时可证明溶液浓度越大,反应速度越快;
故可填.用过氧化氢和二氧化锰制氧气时,该变化是化学反应,可用文字表达式表示为过氧化氢
水+氧气,所以其化学反应方程式是:2H2O2二氧化锰
2H2O+O2↑; MnO2 .
(6)把带火星木条伸入管口内观察:如果木条复燃,说明制取的气体是氧气,否则不是氧气;
故答案是:(1)集气瓶;
(2)催化、2KClO3
2KCl+3O2↑、②、④或⑤;MnO2 . △
(3)③④①②⑤⑥;
(4)B;
(5)①相同条件下,MnO2的催化效果比Fe2O3好,或②在其他条件相同的情况下,H2O2浓度越大,产生氧气的速度越快;2H2O2
2H2O+O2↑; MnO2 .
(6)在集气瓶内伸入带火星的木条,观察木条是否复燃.
